|
|
|
|
|
表明乙型流感病毒宿主范围扩大的证据正日益增多| MDPI Viruses |
|
|
期刊:Viruses
期刊主页:https://www.mdpi.com/journal/viruses
论文链接:https://www.mdpi.com/1999-4915/17/12/1528
论文标题:Mounting Evidence for an Expanded Host Range of Influenza B Viruses
一、研究背景
乙型流感病毒(Influenza B virus, IBV)是每年季节性流感的主要病原体之一,给全球公共卫生带来沉重负担。长期以来,IBV被认为是一种严格局限于人类感染的病毒,缺乏像甲型流感病毒那样广泛的动物宿主库,因此不被认为具有引发大流行的潜力。然而,近年来越来越多的证据表明,IBV具有人畜共患的潜力,可以感染包括家养动物、伴侣动物乃至野生动物在内的多种哺乳动物。与此同时,宏基因组学研究揭示出,在鱼类和两栖动物中存在着与IBV高度相似的“IBV-样病毒”,暗示这类病毒的进化历史远比我们想象的更为古老和复杂,可能与动物宿主存在着长期的共同进化。
二、综述内容
1. 实验模型揭示IBV的潜在宿主范围
实验感染模型是探究病毒宿主范围和传播潜力的关键工具。综述指出,多种哺乳动物,包括雪貂、小鼠、豚鼠、猪、仓鼠和树鼩等,均可在未经病毒适应性传代的情况下被IBV有效感染。其中,雪貂作为流感研究的“金标准”模型,在部分毒株表现出有限的气溶胶传播能力条件下,仍然对IBV高度易感。除此之外,猪不仅能被IBV感染,还会发生猪与猪之间的直接接触传播。这些实验证据表明,IBV感染并非局限于人类,其具备感染多种哺乳动物的内在潜能。然而,能否在这些动物中建立持续传播链,才是判定其是否构成真正动物宿主的关键。因此,评估病毒在动物个体间的持续传播能力,对于理解IBV的生态学至关重要。
2. 动物中IBV感染的证据:从反向人畜共患到鳍足类
除实验感染外,自然界中也积累了大量的IBV感染动物的证据(图1)。自上世纪60年代起,马、猪、狗、非人灵长类等与人类密切接触的动物体内,均检测到针对IBV的抗体,表明存在着频繁的反向人畜共患(reverse zoonosis)事件。其中在美国和中国台湾的猪群中,已成功分离到与同时期人群中流行的IBV高度同源的病毒(>99%相似性),为人类向动物的病毒溢出提供了确凿的分子证据。
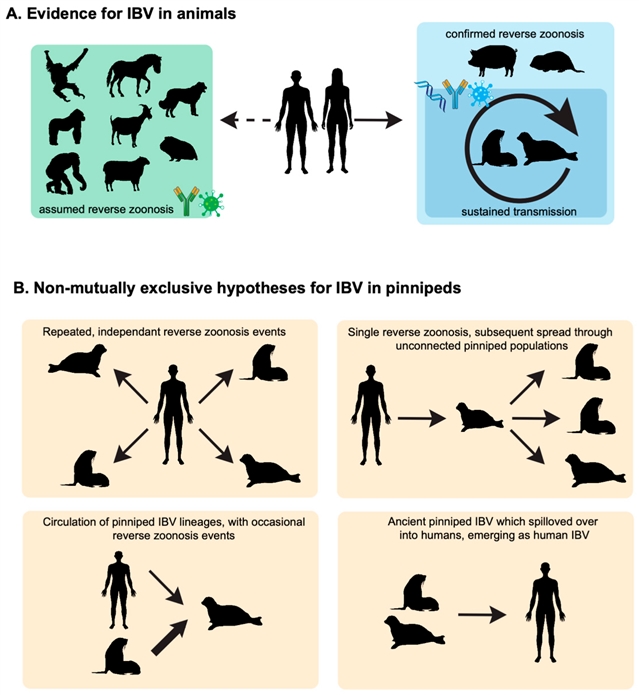
图1. 乙型流感病毒在动物中的生态学与传播假说。
(A)IBV在人群中循环,并通过反向人畜共患事件多次溢出多种动物。(B)关于鳍足类在IBV生态中作用的四种非互斥假说。
自1999年荷兰海豹暴发呼吸道疾病以来,多个研究团队在不同地理区域、不同种类的鳍足类动物(如灰海豹、斑海豹、里海海豹等)中均检测到IBV抗体,且在一只2020年死亡的里海海豹脾脏中通过宏基因组学直接检测到了IBV基因片段。考虑到部分幼年海豹的抗体阳性(提示近期感染),以及抗体阳性样本跨越十余年时间,综述提出了四种假说(图1B):(1)人类向海豹的多次独立溢出事件;(2)一次溢出后在海洋哺乳动物中的持续传播;(3)海豹中存在独立于人类的IBV谱系;(4)海豹是人类IBV的祖先来源。尽管目前尚无基因组学证据支持后两种假说,但这些可能性凸显了我们对IBV生态认知存在空白。
3. 鱼类和两栖动物的IBV-样病毒
宏基因组学技术的兴起改变了病毒的发现模式。研究团队重点介绍了四种与IBV亲缘关系密切但进化上更为古老的病毒:蝾螈流感样病毒(SILV)、武汉刺鳗流感样病毒(WSEIV)、大马哈鱼流感样病毒(CSILV)和暹罗食藻鱼流感样病毒(SAEILV)。这些病毒在基因组结构上与IBV高度相似,更关键的是,通过冷冻电镜和AlphaFold3结构预测,它们的血凝素(HA)蛋白在整体结构上与IBV也非常相似,尽管氨基酸序列相似性仅为27-31%。
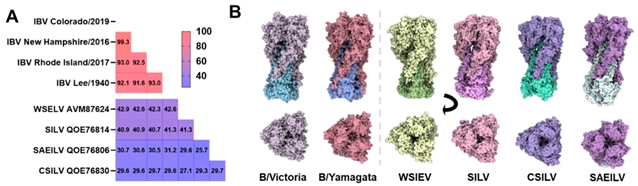
图2. (A) IBV 和 IBV-样病毒血凝素 (HA) 的全局蛋白质序列同一性; (B) IBV 和IBV-样病毒?凝素(HA) 的结构?较。(上排)侧视图;(下排)顶视图。
功能表征则进一步揭示了它们之间的差异:SAEILV和CSILV的HA可识别α2,3-连接的唾液酸受体,类似于禽流感病毒;WSEIV的HA则识别神经节苷脂GM2;而SILV的HA未能与任何受试聚糖结合。这些差异决定了它们各自的宿主偏好性。重要的是,这些IBV-样病毒在抗原性上与人类IBV截然不同,人类血清中不存在交叉中和抗体。尽管如此,IBV-样病毒的神经氨酸酶(NA)仍对奥司他韦等抗流感药物敏感。这些发现为理解IBV的进化起源提供了宝贵视角,表明IBV可能在脊椎动物中拥有悠久的进化历史。
该综述系统梳理了IBV在动物中感染的现有证据,整合了实验感染模型、血清学调查、病毒基因组检测以及对鱼类和两栖动物中IBV-样病毒的功能研究,全面探讨了IBV潜在的宿主范围、跨物种传播机制及其深远的生态学意义。
三、作者介绍
本文通讯作者为墨尔本大学微生物与免疫学系、彼得·多尔蒂感染与免疫研究所的Marios Koutsakos博士。第一作者及共同作者还包括墨尔本大学的Michelle Wille博士以及昆士兰大学化学与分子生物科学学院的Rhys H. Parry博士。该研究得到了澳大利亚国家健康与医学研究理事会及澳大利亚卫生部的资助。
关于期刊 Viruses
Viruses (ISSN 1999-4915, IF 3.5, CiteScore 7.7) 创刊于2009年,是病毒学领域的国际开放获取期刊,专注于病毒感染、病毒分类、病毒-宿主互作、抗病毒治疗、噬菌体、病毒进化与基因组学等研究方向。期刊被 SCIE、PubMed、Scopus、MEDLINE 等权威数据库收录,最新影响因子3.5(JCR Q2),CiteScore 7.7(病毒学/传染病学 Q1)。西班牙病毒学会、意大利病毒学会、加拿大病毒学会等国际学术组织均与 Viruses 达成合作,会员可享受文章处理费折扣。
期刊主页:https://www.mdpi.com/journal/viruses
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。