|
|
|
|
|
同济大学附属东方医院方文涛教授团队研究成果:重审胸腺上皮肿瘤的新辅助治疗策略 | MDPI Cancers |
|
|
论文标题:A Re-Examination of Neoadjuvant Therapy for Thymic Tumors: A Long and Winding Road
论文链接: https://www.mdpi.com/2072-6694/16/9/1680
期刊名:Cancers
期刊主页:https://www.mdpi.com/journal/cancers
通讯作者简介:

方文涛教授
同济大学附属东方医院
方文涛,同济大学附属东方医院胸外科主任、教授、博士生导师
中国抗癌协会纵隔肿瘤专业委员会名誉主任委员、中国抗癌协会食管癌专业委员会副主任委员、中国医药教育协会肺部肿瘤专业委员会副主任委员、中国医师协会胸外科分会常务委员、中华胸心外科学会肺癌专家组委员、上海市医学会外科学组委员;同时担任国际肺癌研究会(IASLC)多学科临床科学委员会委员、胸部肿瘤分期委员会(SPFG)数据质量委员会委员及胸腺肿瘤分期委员会M分期组长、国际胸腺瘤研究会(ITMIG)教育委员会主席、国际食管疾病协会(ISDE)会员、欧洲胸心外科协会(EACTS)胸外科部执行委员会委员、美国胸心外科协会(AATS)会员、亚洲胸心血管外科协会(ASCVTS)胸外科部执行委员会委员、亚洲胸外科学院(ATA)发展部主席。担任《Mediastinum》杂志主编、《Shanghai Chest》执行主编、《Journal of Thoracic Diseases》副主编和《Journal of Thoracic and Cardiovascular Surgery》、《Annals of Thoracic Surgery》、《Chinese Medical Journal》等SCI期刊编委、《中华外科杂志》、《中华胸心血管外科杂志》、《中国胸心血管外科临床杂志》等核心期刊编委。
文章背景
胸腺上皮肿瘤(TETs)是一类罕见的肿瘤,其治疗策略一直是胸外科和肿瘤学领域关注的焦点。肿瘤根治性R0切除被认为是改善预后的关键因素,但对于局部晚期病例,单纯手术往往难以实现R0切除,因此新辅助治疗成为提高切除率的重要手段。新辅助化疗在胸腺瘤中有一定疗效,但在胸腺癌中的有效性及最佳方案仍存在争议。与此同时,放化疗联合、免疫治疗及靶向药物在新辅助阶段的潜力也正逐步被探索。来自东方医院方文涛教授团队在Cancers期刊发表了综述,梳理了现已有的证据,总结了新辅助治疗在胸腺肿瘤治疗中的现状和所面临的挑战,以及未来可能用于临床的选择,希望为临床决策和未来临床研究的开展提供见解。
新辅助化疗:疗效与挑战
目前,化疗是胸腺肿瘤最常用的新辅助治疗模式,其依据主要来源于Kim等人和Kunitoh等人的两项前瞻性、单臂研究的结果。两项研究均展现了较好的OR率(77%、62%)和R0切除率(76%、69%)。OR率和R0切除率的差异可能来源于:Kim等人的研究对于需要新辅助治疗的“不可切除”定义过于宽泛;并且Kim等人所用的诱导化疗法案中含有激素,会导致淋巴细胞丰富的胸腺瘤进一步退缩。此外,由于两项研究的纳入均缺乏胸腺癌的患者,因此对于胸腺癌患者,新辅助化疗的疗效尚不明确。而Hirai等人的研究显示晚期胸腺癌患者化疗的OR率仅为36%。综合以上研究,在未来有关胸腺肿瘤新辅助治疗的研究中:要进一步探索新辅助化疗对胸腺癌的效果或及时为胸腺癌患者寻找更有效的新辅助治疗策略;同制定新辅助治疗的入组标准要更加客观化,以方便不同研究结果的对比解读。
新辅助放化疗:初现曙光
同期放化疗既往只作为无法手术TET患者的根治性治疗,二者联合作为新辅助治疗理论上应该可以起到更强劲使肿瘤退缩的效果。现阶段有关新辅助放化疗的研究较少,Wright等人的回顾性研究中,10例不可切除的TETs患者接受同步放化疗后,80%的患者实现了R0切除,且2位患者达到了近乎完全的病理缓解。在Korst等人的前瞻性研究中,同期放化疗带来了48%的OR率和80.9%的R0切除率,24%的患者治疗后瘤床肿瘤细胞小于10%。在Xu等人的前瞻性研究中,同期放化疗带来了48.5%的和82.6%的R0切除率,且胸腺瘤相比于胸腺癌对于同期放化疗更加敏感(胸腺瘤OR率63.6%,胸腺癌OR率40.9%)。现阶段,新辅助放化疗展现了其潜力,但其应用也面临着几个问题,需要今后的临床研究带来答案。第一,其疗效与化疗的疗效无法进行有效的头对头对比,哪些病人在同期放化疗中获益最大也尚未可知;第二,放化疗的安全性也需要进一步的考虑,通过序贯放化疗是否能规避掉放疗带来的风险和对手术切除的影响也需要探索。
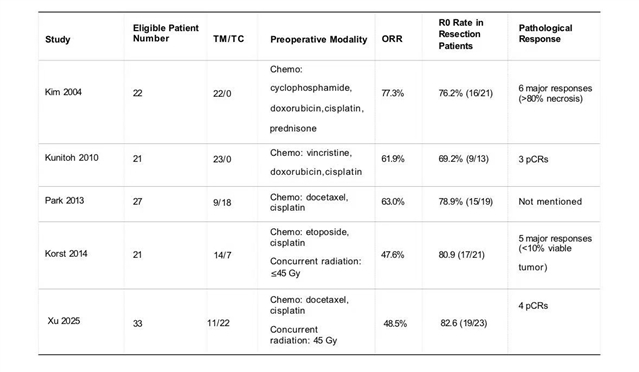
表1:TETs新辅助治疗前瞻性临床研究的有关结果
免疫与靶向治疗:未来可期
近年来,免疫检查点抑制剂(ICIs)和靶向治疗在TETs的治疗中展现出希望。例如,帕博丽珠单抗、阿替利珠单抗在晚期TETs患者的二线治疗中显示出较好的客观缓解率,但由于在胸腺瘤患者中使用存在着较高的免疫相关不良事件风险,现只推荐其在胸腺癌患者中治疗使用。此外,靶向治疗药物在晚期胸腺癌的二线治疗中也展现了较好的疗效,如舒尼替尼(OR率:26%)、仑伐替尼(OR率:36%)、阿帕替尼(OR率:40%);而近期于CSCO年会上公布的有关德立替尼用于二线或后线晚期胸腺癌的多中心、随机、双盲、对照II期临床研究结果展现了德立替尼在PFS和ORR上均优于安慰剂。免疫治疗和靶向治疗在晚期TETs的二线治疗中展现的疗效,也催生了不少研究其在晚期一线甚至新辅助场景应用的临床试验,部分中心也积攒了一定量的免疫治疗应用于TET术前治疗的案例,Hao等人于2023年WCLC年会汇报了12例经经免疫治疗后行手术切除的胸腺肿瘤案例,在其中九例的胸腺癌患者中,免疫治疗作为一线新辅助治疗的OR率高达55.6%;总体病人的R0切除率为66.7%。未来,随着免疫治疗和靶向治疗药物在胸腺肿瘤治疗中的应用场景越来越多,如何有效的进行疗效预测以及病人筛选将成为重点。
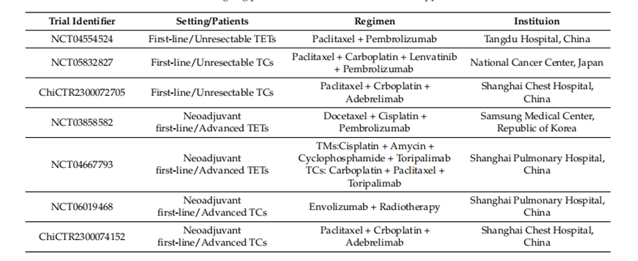
表2:正在进行的免疫治疗用于TET一线治疗的临床试验
文章结语
对于TETs这样罕见的肿瘤来说,高质量随机对照研究难以开展,当前的治疗策略更多依赖于既往的回顾性及前瞻性研究所提供的证据。这些研究虽已为术前治疗奠定了基础,但目前仍难以断言哪种路径最优,且不能满足部分病人的治疗需求,探索仍在继续。
尽管新辅助化疗目前是胸腺瘤患者最有效的术前治疗方式之一,但对于胸腺癌,其效果仍需更多研究加以确认。同时,关于同步或序贯放化疗的安全性和疗效,也有待进一步的临床证据支持。免疫治疗和靶向治疗在新辅助阶段的应用正在临床试验中探索,希望在未来的十年未局部晚期的TET患者带来新的希望。与此同时,我们还需对TETs的生物学本质有更深入、全面的理解,探索新的治疗靶点,才能为今后的临床实践提供更科学的依据。
原文出自 Cancers 期刊
Yu, F.; Gu, Z.; Zhang, X.; Xu, N.; Hao, X.; Wang, C.; Zhao, Y.; Mao, T.; Fang, W. A Re-Examination of Neoadjuvant Therapy for Thymic Tumors: A Long and Winding Road.Cancers 2024, 16, 1680.

推文链接:https://mp.weixin.qq.com/s/2BKF1x3kfoTPhA7u-Pa64A
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。