|
|
|
|
|
微纳3D打印撬动医学未来:从精准输送到仿生器械的全链革新 |
|
|
微纳加工技术正深刻重塑生物医学工程的基础构建方式与治疗机制。近年来,随着材料学、药物递送、组织工程等多学科的交叉融合,微纳3D打印在高精度构型控制能力、结构设计自由度、多材料兼容性等优势,为个性化医疗与精准治疗落地提供强有力的技术支持。
近期,发表于 ACS Nano、Advanced Science 和 Chemical Engineering Journal 的三项前沿研究,系统展示了摩方精密微纳3D打印技术在抗肿瘤耐药治疗、仿生抗菌微针设计以及干细胞功能敷料构建等方向的最新成果。这些研究不仅证明了微纳3D打印技术在复杂医疗需求中的实用性,也体现在构建下一代诊疗体系中的核心价值。
ACS Nano:微针手术刀,打破乳腺癌耐药困局
武汉大学药学院黎威教授团队与武汉大学生命科学学院宋质银教授团队合作,提出一种创新策略——基于线粒体靶向微针(HDT-Z@MNs)系统,精准激活癌细胞“死亡开关”,打破乳腺癌阿霉素耐药困局。研究团队首先合成了DOX-TPP@ZIF-67 NPs。首先,将硝酸钴和2-甲基咪唑在水中反应,形成紫色的ZIF-67纳米颗粒。然后将带有三苯基膦(TPP)的DOX溶于水中,加入到ZIF-67中,利用其孔结构和表面电荷吸附药物,在pH约6.5–7的条件下反应72小时,获得中空结构的DOX-TPP@ZIF-67 NPs。TEM和SEM图像显示颗粒约为210 nm;N2吸附-脱附测试显示具有介孔结构,表明药物已装载;装药后比表面积与孔体积略有降低,验证了载药效果;BJH分析显示孔径集中在约2 nm和60 nm。ZIF-67的钴离子中心具有催化分解H2O2的功能,可使纳米粒子在富含H2O2的环境中实现推进;在不同浓度H2O2中观察到粒子运动轨迹增强、扩散速率增快、均方位移(MSD)升高;表明其可作为“纳米马达”,在肿瘤等富H2O2微环境中增强药物富集。药物释放在酸性环境(pH 5.5)和高H2O2浓度下显著加快;表明其具有pH和H2O2响应性,适合于肿瘤微环境中的靶向药物释放。
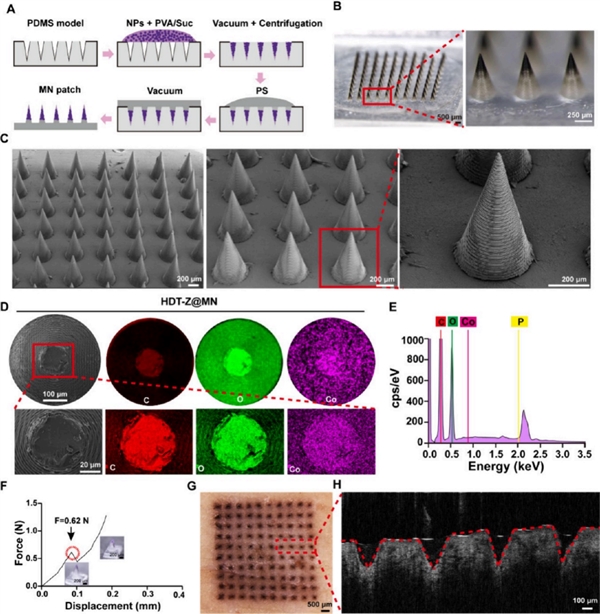
图: 中空DOX-TPP@ZIF-67纳米颗粒负载纳米颗粒的表征(HDT-Z@MNs)
实验所需该微针阵列由摩方精密microArch S240 (精度:10 μm)3D打印设备加工,后经PDMS翻模制备而成的。这项研究不仅展示了微针系统的高度可控性与安全性,也提出了以线粒体为新兴靶点的多重协同治疗策略,为乳腺癌及其他耐药性实体瘤的临床治疗提供了新方向。
Advanced Science:果蝇仿生微针贴片,高效促治疗
细菌感染性口炎(BIS)是一种常见的口腔黏膜炎症性疾病,主要由链球菌、葡萄球菌等致病菌引发,临床常表现为黏膜红肿、剧烈疼痛、反复性溃疡及继发感染等症状。尽管传统治疗主要依赖局部消炎、镇痛与抗菌药物,但口腔环境复杂、动态变化剧烈,药物递送常常受限于唾液冲刷、黏膜屏障及溃疡表面假膜的阻隔,导致治疗效果不稳定、复发率高。这一难题,正促使口腔治疗手段从单一药物干预转向结构材料与递送路径协同优化的新阶段。
针对口腔环境的动态特性与治疗需求,水凝胶材料因其良好的生物相容性、高含水性及易于药物负载与改性,近年来在局部口腔治疗中备受关注。通过引入仿生设计理念,水凝胶可进一步构建成具微针结构的贴片装置,实现对病灶区域的稳定附着与定向释放。由兰州大学范增杰教授团队研发的一种仿生微针贴片系统,受果蝇跗节吸附结构启发,融合温敏抗菌水凝胶与仿生吸盘设计,实现了在湿润口腔环境中的高附着、高效控释和局部抗炎协同治疗,在动物模型中展现出显著的组织修复与炎症抑制效果,标志着功能型微结构在复杂口腔环境中精准干预的可行路径。
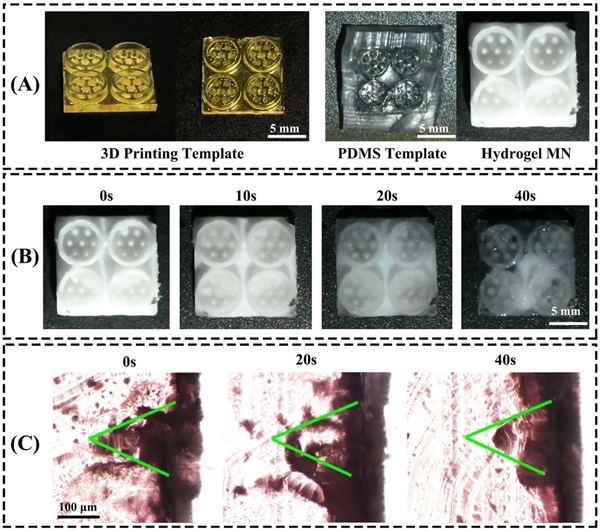
图:MN 吸盘的表征
该新型仿生微针贴片的关键结构——吸附式微针阵列,使用摩方精密面投影微立体光刻技术(PμSL)进行模板加工。采用高精度3D打印系统: microArch S230(精度达2μm),研究团队得以精准复刻果蝇爪部吸盘的微观结构,实现仿生贴片在亚结构尺度上的几何还原与形貌控制。这种高分辨率、高重复性的加工能力为微结构仿生功能化提供了基础保障,也为口腔微环境中高附着力、高稳定性治疗器械的规模化研发打开了新思路。
论文链接:https://doi.org/10.1002/advs.202500432
Chemical Engineering Journal: 干细胞球创可贴加速伤口愈合
间充质干细胞(MSCs)在免疫调节与组织再生中的治疗潜力已被广泛验证,尤其在炎症控制和创面修复领域展现出显著优势。相较于悬浮形式的干细胞,结构稳定、旁分泌功能更强的干细胞球(mesenspheres)正成为新一代治疗策略的重要方向。然而,传统以注射为主的递送方式存在侵入性强、局部保留率低等问题,严重制约了其临床应用效率。因此,探索一种非侵入式、可控释放、可多次使用的干细胞递送平台,已成为再生医学技术转化的关键任务。
针对当前干细胞球敷料在成球效率、分布均匀性、释放完整性与重复给药能力等方面的技术瓶颈,澳门大学最新研究中提出了一种创新型干细胞球敷料(MSB,Mesensphere Sheet Bandage)解决方案。该敷料基于可图案化微孔的PDMS(聚二甲基硅氧烷)材料设计,不仅可实现干细胞球的高通量自组装与均匀释放,还具备多次贴敷与常温保存能力。实验证实,该敷料在提升干细胞因子分泌水平的同时,可显著加快小鼠模型创面愈合速度(+33%),并提升皮肤再生组织的结构完整性(+58%),展现出极强的临床应用潜力,尤其适用于糖尿病足溃疡、烧伤等慢性创伤治疗。
MSB敷料的核心制造环节,研究团队采用microArch® S240设备(精度10μm)构建微柱阵列模具,并通过PDMS浇注复制出成千上万个高密度微孔结构。该结构不仅实现干细胞悬液在微尺度空间内的自发聚集成球,还具备一致性强、制备通量高、操作简便等优势,形成了从干细胞球制备、敷料构建到临床贴敷的完整链条。摩方精密的高分辨率打印能力与材料适配性,为该项创新成果提供了关键制造支撑,也为再生医学器械从实验室走向规模化临床应用构筑了坚实基础。
论文链接:https://doi.org/10.1016/j.cej.2025.164346
微纳3D打印不仅限于单一结构的构建工具,其所带来的治疗精准化、器械智能化、生产定制化趋势,将深刻改变传统医疗创新研发范式,为精准医疗、再生医学和个性化治疗开辟全新边界。
摩方精密深耕微纳3D打印行业,用微米级技术扎根微观世界,从提升抗药性治疗效率、优化创伤修复路径,到实现组织再生的精确控制,正成为连接基础研究与应用医学之间的关键枢纽。未来,摩方也将持续拓展生命健康的技术边界,推动多学科协同创新,助力医疗产业向更安全、个性化、智能化方向发展。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。