|
|
|
|
|
膜蛋白研究的“清道夫”:新方法既去SDS,又保蛋白完整 | MDPI Proteomes |
|
|
期刊名:Proteomes
期刊主页:https://www.mdpi.com/journal/proteomes
在蛋白质组学研究中,十二烷基硫酸钠(SDS)是一种常用的表面活性剂,主要用于细胞裂解、蛋白提取,尤其是溶解疏水的膜蛋白成分——这些蛋白在纯水溶液中难以回收。然而,SDS也是一把“双刃剑”:即使浓度很低,也会严重干扰下游的蛋白处理和质谱分析,包括抑制胰蛋白酶消化、破坏反相色谱分离、抑制电喷雾离子化效率等。
因此,研究者面临一个两难困境:膜蛋白需要SDS来溶解,但SDS又必须在质谱分析前去除。如何在去除SDS的同时,保持膜蛋白的完整性和溶解性?这是膜蛋白质组学样品制备环节长期面临的挑战。
一、KCl沉淀法:一个巧妙的解决方案
SDS Depletion from Intact Membrane Proteins by KCl Precipitation Ahead of Mass Spectrometry Analysis
质谱分析前用KCl沉淀法去除完整膜蛋白的SDS
https://www.mdpi.com/2227-7382/13/3/30
近期在Proteomes发表的这篇文章,研究团队来自加拿大达尔豪西大学,他们系统评估了用KCl沉淀去除SDS的最佳条件。研究发现,在强碱性条件(pH 12)下加入尿素,再向含SDS的膜蛋白溶液中加入KCl,SDS会与K+形成不溶性沉淀,通过离心即可去除。而膜蛋白由于保持在碱性尿素环境中,仍然保持溶解状态。
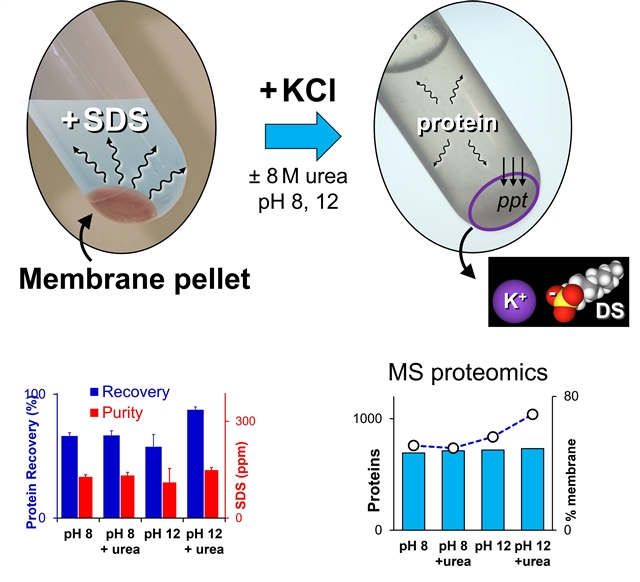
研究使用菠菜叶绿体和肝脏膜蛋白作为模型样本。质谱分析结果显示,在优化的条件下(pH 12+尿素),鉴定到的蛋白中69.3%为膜蛋白,共732种膜蛋白被成功鉴定。更重要的是,质谱图显示信号清晰,完全没有SDS加合物的干扰。
研究者还比较了不同pH条件下的效果:pH 8不加尿素时,鉴定到的蛋白总数更多,但膜蛋白占比更低;而pH 12加尿素虽然总鉴定数略少,但膜蛋白的回收率和纯度最高。这表明,如果研究目标是膜蛋白,强碱性条件加尿素是最佳选择。
二、两种SDS去除技术的对比
如果您也在为膜蛋白样品的SDS去除寻找方法,除了上述KCl沉淀法,还可以关注另一种技术路线--电泳 depletion方法,下面文章对此进行了系统性研究。
Enhanced Electrophoretic Depletion of Sodium Dodecyl Sulfate with Methanol for Membrane Proteome Analysis by Mass Spectrometry
甲醇强化电泳损耗用于膜蛋白质组质谱分析
https://www.mdpi.com/2227-7382/12/1/5
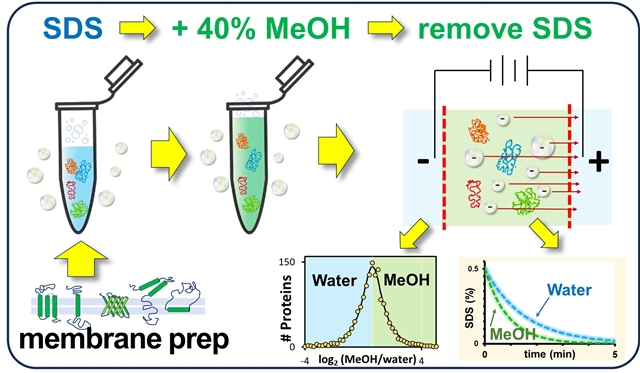
该方法利用透析管电泳装置,在电场作用下驱动带负电的SDS分子向正极迁移,穿过透析膜进入外部缓冲液。研究者发现,在电泳过程中加入20-30%的甲醇,可以有效维持疏水蛋白的溶解性,避免蛋白沉淀损失。
优化后的方法处理大肠杆菌膜蛋白样品,可鉴定到412种膜蛋白,占鉴定蛋白总数的47%,其中包含多次跨膜蛋白。与传统丙酮沉淀法相比,蛋白回收率从60%提升至85%,膜蛋白占比从25%提升至47%。
两种方法各有优势:
•KCl沉淀法:操作简单、成本低,无需特殊设备,适合常规实验室
•电泳法:去除更彻底,适合极低丰度样品,但需要专用装置
研究者可根据自己的实验条件和研究目的选择合适的方法。
三、延伸阅读:翻译后修饰检测方法
Uncovering Enzyme-Specific Post-Translational Modifications: An Overview of Current Methods
揭示酶特异性翻译后修饰:当前方法综述
http://www.mdpi.com/2227-7382/13/3/37
文章指出,PTM(Post-Translational Modifications)是蛋白质功能调控的关键,目前已发现超600种修饰类型,其中磷酸化、乙酰化、泛素化占比超90%。这些修饰由“写入酶”和“擦除酶”介导,解析酶-底物关系是研究难点,也是功能蛋白质组学的核心任务。
文章将酶特异性PTM底物发现方法分为三类:
•体外方法:基于蛋白/肽阵列、SPOT合成等技术,可快速筛选酶的识别序列,是底物发现的探索性手段,但难以模拟细胞内真实环境。
•细胞基方法:依托质谱技术为核心,结合抗体富集、邻近标记等策略,能在生理背景下解析酶-底物网络,是目前的主流研究手段。
•计算方法:涵盖机器学习、深度学习等技术,可实现PTM位点和酶特异性底物的高通量预测,实验与计算结合的混合方法是领域重要发展趋势。
当前研究面临高质量酶特异性数据缺乏、PTM定位误差等挑战。未来需将精密计算策略与实验技术深度整合,借助人工智能和高通量分析,进一步解析复杂的PTM酶-底物网络。
Proteomes 期刊介绍
主编:Jens R. Coorssen, Brock University, Canada; Matthew P. Padula, The University of Technology Sydney, Australia
期刊专注于蛋白质组分析的各个方面,特别关注蛋白质组在蛋白质形式(proteoforms)、功能性生物学单元以及标准氨基酸序列水平上的定量和表征。目前已被Scopus、ESCI (Web of Science)、PubMed等数据库收录。
2024 Impact Factor: 3.6
2024 CiteScore: 7.2
Time to First Decision: 28.6 Days
Acceptance to Publication: 5.6 Days
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。