|
|
|
|
|
首尔大学Seung-Yong Seong教授团队-高强度聚焦超声增强CCL19/21介导的树突状细胞疫苗在肿瘤微环境中的疗效 | MDPI Pharmaceutics |
|
|
论文标题:HIFU-CCL19/21 Axis Enhances Dendritic Cell Vaccine Efficacy in the Tumor Microenvironment
论文链接:https://doi.org/10.3390/pharmaceutics17010065
期刊名:Pharmaceutics
期刊主页:https://www.mdpi.com/journal/pharmaceutics
课题简介
有效靶向治疗耐药肿瘤细胞,特别是参与肿瘤复发的癌症干细胞(CSCs),仍然是免疫治疗领域的一项重大挑战。首尔大学 Seung-Yong Seong 教授团队在Pharmaceutics发表的这项研究,探讨了将机械式高强度聚焦超声(M-HIFU)与树突状细胞(DC)疫苗联合应用,以增强针对表达OLFM4肿瘤(一种与免疫逃逸和肿瘤生长相关的CSC标志物)的免疫反应的潜力。采用M-HIFU通过机械性破坏肿瘤细胞,释放肿瘤相关抗原并创造免疫刺激环境,从而诱导免疫原性细胞死亡。随后,接种负载OLFM4的DC疫苗,以增强该预激活环境下的免疫反应。M?HIFU 与 DC 疫苗联用可显著抑制肿瘤生长与转移,并通过上调趋化因子 CCL19 和 CCL21 增强 T 细胞活化、促进免疫细胞募集。这种协同作用增强了免疫记忆,降低了肿瘤复发的可能性。
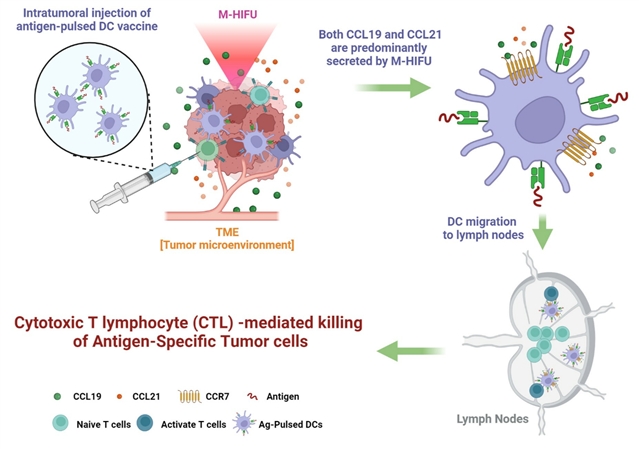
研究过程与结果
实验首先通过皮下注射肿瘤细胞建立荷瘤小鼠模型,并从骨髓前体细胞中诱导分化DC,经OLFM4蛋白负载后制备DC疫苗。研究分别采用热消融 HIFU(T-HIFU)与机械消融 HIFU(M-HIFU)对肿瘤进行处理并对比其免疫效应。
为了验证治疗效果,课题组进行了一系列免疫学检测:与T-HIFU治疗组相比,M-HIFU治疗组小鼠的肿瘤生长显著延迟。M-HIFU组小鼠脾脏中OLFM4特异性产生IFN-γ的细胞数量显著高于T-HIFU组或NC组,M-HIFU在荷瘤小鼠中诱导了更强的OLFM4特异性免疫反应。采用 ELISA 检测显示,肿瘤部位趋化因子 CCL19 和 CCL21 的蛋白水平显著升高,尤其是在 M-HIFU 治疗组中。这种趋化因子表达的升高重塑了肿瘤微环境,能够更有效地促进 DC 迁移,增强抗肿瘤免疫应答。此外,还统计了肺部可见肿瘤结节的数量,结果显示瘤内注射 DC 疫苗联合 M-HIFU(DCs [IT] + M-HIFU)组的肺转移结节数量显著低于皮下注射 DC 疫苗联合 M-HIFU(DCs [SC] + M-HIFU)组,进一步支持了 M-HIFU 在该模型中增强抗肿瘤疗效的假设。
综上,M-HIFU 与 DC 疫苗的这种协同作用可产生更强、更持久的抗肿瘤免疫反应,而 T-HIFU 由于其热效应和可能诱导免疫抑制微环境,则难以达到这种效果。
研究总结
本研究探讨了机械性高强度聚焦超声(M?HIFU)联合树突状细胞(DC)疫苗在肿瘤治疗中的协同效应。M?HIFU 通过机械破坏肿瘤组织,促进肿瘤抗原及趋化因子 CCL19/CCL21 释放,相较于热消融性 HIFU(T?HIFU)可诱导更强的抗肿瘤免疫应答。该联合疗法在消除原发瘤的同时抑制转移,与免疫检查点抑制剂或 CAR?T 疗法具有协同潜力。未来需优化治疗参数并在多种肿瘤模型中验证其安全性与有效性。
期刊介绍
主编:Patrick J. Sinko, Rutgers University, USA
期刊领域涵盖生物制药、药物递送、药物控释、药物制剂、药物靶向、药代动力学、纳米医学、药物遗传学、药物基因组学、药效学等。目前期刊已被SCIE、Scopus和PubMed等数据库收录,位列JCR“药理学与药学”学科领域Q1区。
2024 Impact Factor:5.5
2024 CiteScore:10.0
Time to First Decision:15.7 Days
Acceptance to Publication:3.5 Days
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。