|
|
|
|
|
佐治亚大学——体外精子发生研究的最新进展及未来方向 | MDPI Reproductive Medicine |
|
|
论文标题:Recent Developments in In Vitro Spermatogenesis and Future Directions
论文链接:https://doi.org/10.3390/reprodmed4030020
期刊名:Reproductive Medicine
期刊主页:https://www.mdpi.com/journal/reprodmed
在生殖生物学领域,精子发生(spermatogenesis)长期被认为是最复杂、最精细、也最难以在体外重现的发育过程之一。其发生依赖于睾丸高度特化的微环境:支持细胞(Sertoli cells)提供结构与营养支撑,间质细胞(Leydig cells)调控激素信号,管周肌样细胞维持组织结构完整性,多种细胞类型在空间与时间上精密协调,共同完成精原干细胞(SSCs)向功能性精子的分化过程。
正因如此,“体外精子发生”(in vitro spermatogenesis, IVS)在相当长时间内被视为理论可行但技术上难以真正实现的目标。
然而,近年来随着诱导多能干细胞(iPSCs)技术成熟、三维培养体系发展、类器官技术兴起以及减数分裂调控机制的深入解析,这一局面正在发生实质性改变。
来自 University of Georgia 的 Dr. Charles A. Easley 团队在 Reproductive Medicine 发表的最新综述,对过去两年非小鼠体系中IVS的关键进展进行了系统性总结。该文不仅梳理了不同技术路径的实验进展,更重要的是,展示了IVS如何从“概念探索”逐步转向“可工程化优化的技术体系”。
这或许是该领域真正意义上的阶段性转折。
一、雄性生殖细胞发育
哺乳动物雄性生殖细胞发育始于胚胎期,原始生殖细胞(PGCs)由上胚层诱导形成并迁移至生殖嵴,在发育过程中经历广泛表观遗传重编程。出生后,前精原细胞分化为精原干细胞(SSCs),青春期在激素和微环境信号调控下启动精子发生。该过程包括精原细胞自我更新与分化、减数分裂及精子形成,最终生成成熟精子。尽管精子发生在脊椎动物中具有进化保守性,但啮齿类与灵长类在人类相关模型中存在显著差异,包括分裂次数、发育周期、减数分裂时序、激素依赖方式、精子形态及基因表达谱等。此外,组蛋白向精蛋白转换比例、DNA甲基化水平及印记基因数量也存在物种差异。深入理解这些差异对于建立更准确的人类精子发生模型、推进男性不育研究及开发生殖干预策略具有重要意义。
二、体外器官/组织培养
在体外精子发生(IVS)研究中,离体器官/组织培养(ex vivo culture)仍是目前最接近体内生理环境、也是应用最广泛的技术路径之一。研究表明,在适当培养条件下,离体睾丸组织能够在体外维持一定程度的生精活动,例如在山羊睾丸组织培养体系中已观察到伸长精子或具有尾部的精子样细胞。同时,人类无精症或隐睾患者来源的睾丸组织在含多种生长因子和激素的培养体系中也可产生减数分裂相关细胞,显示出潜在的临床应用前景。然而,在更接近人类的非人灵长类模型中,精原干细胞的分离、长期扩增及稳定分化仍然面临明显技术挑战。因此,如何在体外重建稳定的生精微环境,仍是推动IVS技术进一步发展的关键问题。
三、生物反应器
生物反应器为体外精子发生(IVS)研究提供了一种能够精确控制温度、pH、氧气和营养供给的动态培养平台。近年来,研究者开始利用微型旋转生物反应器构建更复杂的三维类器官体系。例如,有研究利用人类胚胎干细胞在生物反应器中诱导形成三维类器官结构,模拟了生殖嵴及早期性腺发育过程,并观察到多种性腺相关标志物及类血管结构的出现,显示出一定的组织自组织能力。然而,该体系尚未检测到关键的生殖细胞标志物,如OCT4和DAZL,说明其仍停留在早期性腺发育阶段。总体来看,生物反应器为构建复杂的生精微环境提供了新的技术路径,但其在诱导完整生殖细胞谱系形成方面仍需进一步优化
四、微流控系统
微流控系统通过微米级通道精确调控培养环境,可在体外模拟精子发生所需的激素、营养及代谢条件,并通过可控液流持续提供养分并清除代谢废物。研究比较了多种猪睾丸组织培养方式,发现结合琼脂糖凝胶与聚二甲基硅氧烷(PDMS)腔室的体系能够在一定程度上提高减数分裂及后减数分裂生殖细胞的数量,显示出微流控技术在优化体外精子发生培养环境方面的潜在价值。
五、类器官
类器官(organoid)是一种在三维培养体系中形成的“微型器官”,能够在体外部分重建组织结构和功能,被视为连接传统二维细胞培养与整体器官研究的重要桥梁。在体外精子发生(IVS)研究中,睾丸类器官通过自组织形成类似曲细精管和间质区的结构,在一定程度上保留细胞–细胞相互作用及微环境信号,从而更接近体内的生理状态。近年来的研究表明,在小鼠和猪等模型中,类器官体系已能够支持部分甚至完整的精子发生过程;在人类及灵长类研究中,也已实现早期生殖细胞样细胞的形成及睾丸结构的部分重建。然而,目前类器官体系在分化效率、细胞成熟度及培养条件稳定性方面仍存在明显挑战。总体而言,睾丸类器官为解析精子发生机制和探索男性不育治疗提供了重要实验平台,但其向稳定、高效的人体IVS体系转化仍需进一步优化与验证。
六、支架
支架在体外精子发生研究中起着关键作用,它们为精原干细胞(SSCs)提供三维结构,模拟睾丸的自然环境。这些支架不仅支持细胞附着、增殖和相互作用,还允许营养物质和信号分子的有效扩散。常用的细胞外基质(ECM)成分包括胶原蛋白、层粘连蛋白、纤维连接蛋白、明胶和Matrigel,它们帮助再现复杂的组织环境并引导细胞分化。近期研究探索了多种创新支架系统以促进体外精子成熟。例如,研究者使用去细胞化的人睾丸组织结合富血小板血浆,显著提高了SSCs的存活率并促进了关键生殖标记物的表达。另一种方法采用分层的琼脂糖-层粘连蛋白三维培养体系,经过74天培养,SSCs逐渐发育形成具有尾部和典型微管结构的类精子细胞。这些研究表明,精心设计的支架结合特定生长因子和激素,可以在实验室中模拟体内条件,支持人类精子发生的研究。
七、未来方向
尽管体外精子发生和睾丸类器官(organoid)研究取得了显著进展,但仍面临诸多挑战,例如如何提高培养效率、生成功能性精子以及建立可重复、可扩展的实验流程。同时,使用人类睾丸组织进行研究也涉及伦理和监管问题。最新的单细胞研究揭示了精曲小管内细胞之间复杂的相互作用,以及多种因子在精子发生中的重要性。因此,未来研究需要进一步探索将干细胞与支持精子发生的睾丸体细胞(如Sertoli细胞)共同培养的共培养方法,但这种方法可能导致实验结果的变异性,并受到伦理限制。
另一条前沿方向是“分步分化法”,通过模拟体内发育过程,将多能干细胞或体细胞依次诱导为原始生殖细胞样细胞(PGC-like cells)、精原细胞、精母细胞,最终生成精子样细胞。这一方法利用多种生长因子和激素(如BMP4、bFGF、RA、Kit配体、FSH和hCG)精确调控转录和表观遗传过程,已在啮齿动物和灵长类模型中成功生成可受精的功能性精子,并产生健康后代。尽管取得了这些进展,实现功能性人类精子体外生成仍需优化培养条件、明确关键信号通路,并解决伦理问题。未来的研究可能通过结合多种方法,提供更精确的时空信号,从而更接近体外生成成熟精子的目标(图1)。
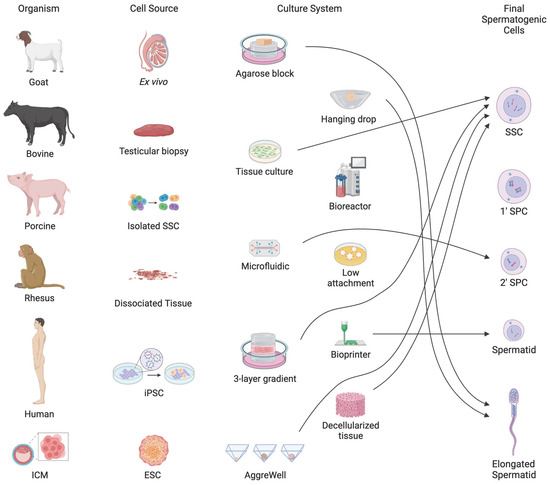
图1. 本文综述了实现体外精子发生的不同方法。
八、结论
IVS研究具有潜在的革命性意义,不仅可能改变生殖医学,也对遗传学研究、药物开发和毒理学检测有深远影响。最直接的应用是在男性不育治疗方面:通过在体外生成成熟精子,即使是精子数量极少、质量不佳或因疾病治疗而失去生育能力的男性,也有可能成为生物学父亲。此外,IVS还为接受化疗等可能损害生育能力的年轻男性提供了保存生育力的新途径,从而减轻生育问题带来的身体、心理和情感压力。
目前,体外睾丸类器官(testicular organoids, TOs)和其他新兴技术(如生物打印、微流控系统)已经能够在实验室中模拟睾丸微环境,推动精子成熟的研究。虽然现有的外植器官或组织培养系统已在部分非啮齿动物中实现完整精子发生,但持续、可控地生成成熟精子仍面临挑战。未来,通过优化类器官及其他先进方法,有望提高分化效率,实现功能性精子的稳定生成。总体来看,IVS是一个前景广阔但仍充满挑战的研究领域,它不仅为男性不育治疗和生育力保存提供希望,也将推动基础生物学和药物研究的发展。
Reproductive Medicine期刊介绍
主编:Prof. Dr. Berthold Huppertz, Medical University of Graz, Austria
期刊研究范围涵盖生殖医学细胞生物学、分子生物学、(表观)遗传学以及生理学和形态学等领域。期刊现已被ESCI、Scopus等数据库收录。
2024 Impact Factor: 1.3
Indexed in Scopus
Time to First Decision: 26.3 days
Acceptance to Publication: 6 days
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。