|
|
|
|
|
自身免疫性肝炎管理:最新进展与未来展望| MDPI Livers |
|
|
论文标题:Autoimmune Hepatitis Management: Recent Advances and Future Prospects
论文链接: https://www.mdpi.com/2673-4389/4/2/17
期刊名:Livers
期刊主页: https://www.mdpi.com/journal/livers
文章导读:
自身免疫性肝炎(AIH)是一种病因未明的慢性肝脏炎症性疾病,临床表现多样,可表现为急性肝衰竭或进展至肝硬化。典型特征为血清免疫球蛋白(以IgG为主)升高,并对类固醇治疗产生应答。20世纪后期,AIH被确认为慢性肝病的一种类型,早期使用皮质类固醇单药或联合硫唑嘌呤治疗可改善患者生存率。近年来,AIH发病率波动于0.4-2.39/10万人年,患病率介于4.8-42.9/10万人。这种差异可能与诊断困难有关,在资源有限地区主要依赖国际自身免疫性肝炎小组(IAIHG)的评分系统进行诊断。目前研究正致力于开发更可靠的诊断方法。标准治疗方案采用皮质类固醇诱导缓解后,联合硫唑嘌呤维持治疗。一线治疗无效时可选用其他免疫抑制剂作为二线方案。治疗目标是实现生化缓解,即肝酶和IgG水平恢复正常。治疗需个体化调整并监测药物副作用。本文综述AIH的发病机制研究进展、诊断标志物开发现状,以及现有和研发中的治疗方案。
发病机制假说:
AIH 的发病机制起始于树突状细胞识别自身抗原肽,该抗原暴露与共刺激信号使初始 CD4+ T 细胞在细胞因子影响下分化为不同 Th 亚群;IL-12 激活主要位于肝实质的 NK 细胞,影响纤维化、肿瘤形成并促进肝脏炎症与组织损伤,IL-4 诱导 Th2 形成,TGF-β 在 IL-12 存在时促使 Treg 和 Th17 由初始 Th0 分化。Treg(CD8+ 和 CD4+/CD25+)在 AIH 中显著减少,外周和肝组织 FOXP3 水平降低,其抑制功能减弱导致免疫细胞与细胞因子失衡;Th17/Th22 水平升高,使 IL-22、IL-13、IL-17、IFN-γ 和颗粒酶 B16 产生增加,IL-17 进一步诱导 IL-6 和 TNF-α 持续放大自身免疫反应。
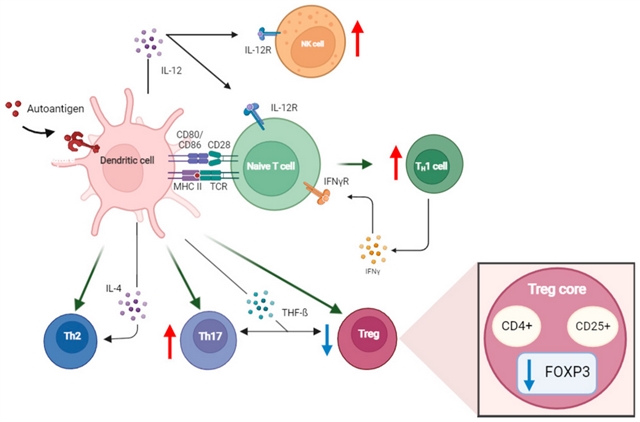
图 1. 自身免疫性肝炎发病机制
疾病管理:
大多数新诊断的AIH患者都需要治疗。治疗指征包括肝酶升高、肝活检显示活动性肝炎或炎症性肝硬化,或肝酶超过正常上限两倍并伴有症状或高胆红素血症。初始治疗目标是诱导缓解,标准为:肝酶(转氨酶和胆红素)恢复正常、血清丙种球蛋白水平正常化、临床症状消失,以及肝组织学炎症改善。一线治疗推荐免疫抑制疗法,可选择单用皮质类固醇或低剂量皮质类固醇联合硫唑嘌呤。2019年AASLD指南建议成人泼尼松单药剂量40-60 mg/天,或与硫唑嘌呤联用时降至20-40 mg/天;部分医疗中心采用1 mg/kg起始剂量,待反应良好后减量。2015年EASL指南推荐初始剂量0.5-1 mg/kg/天泼尼松,随后过渡至50 mg/天硫唑嘌呤。若4-8周后生化指标改善,可逐步减少类固醇,缓解后可尝试停药。若缓解维持12-24个月,可考虑停用硫唑嘌呤(如有使用)。治疗反应存在个体差异,部分患者在7-14天内出现早期应答,而部分需8周以上才显现。获得缓解的患者生存率与普通人群相近,且缓解维持时间越长,总体生存率越高。
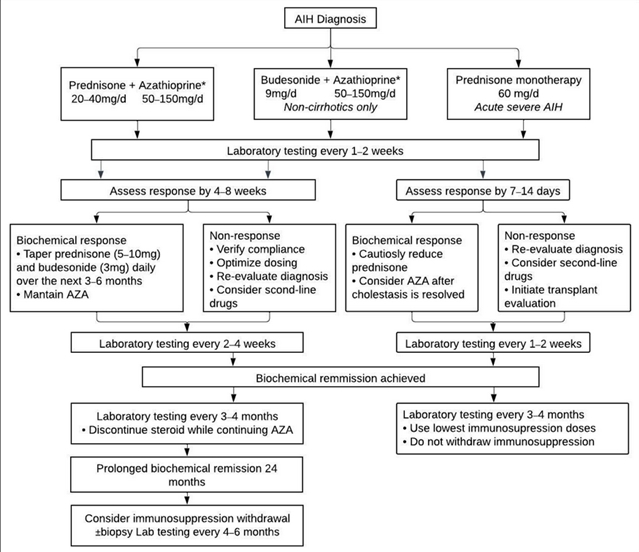
图2 AIH 的一线治疗
总结:
准确及时诊断和有效治疗对改善 AIH 症状及实现生化缓解至关重要,可降低疾病进展和肝移植需求;诱导治疗采用泼尼松或布地奈德联合硫唑嘌呤,用药前须评估 TPMT 活性,定期监测治疗反应后可在生化持续改善时逐步减量;肝移植后继续低剂量免疫抑制并在耐受时停皮质类固醇;治疗失败、无反应或药物不耐受者可使用二线方案,需前瞻性多中心研究确定难治病例最佳方案;合并代谢综合征需处理,因它会对AIH患者的生活质量产生负面影响。

识别二维码,免费阅读英文原文。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。