|
|
|
|
|
仿生巨噬细胞颗粒为治疗耐药菌感染带来新希望 Engineering |
|
|
论文标题:Biomimetic Macrophage–Fe3O4@PLGA Particle-Triggered Intelligent Catalysis for Killing Multidrug-Resistant Escherichia coli
期刊:Engineering
DOI:https://doi.org/10.1016/j.eng.2023.05.022
微信链接:点击此处阅读微信文章

来自天津大学、北京大学等机构的研究人员在中国工程院院刊《Engineering》发表了题为“Biomimetic Macrophage– Fe3O4@PLGA Particle-Triggered Intelligent Catalysis for Killing Multidrug-Resistant Escherichia coli”(仿生巨噬细胞 Fe3O4@PLGA颗粒触发智能催化技术杀灭多重耐药大肠杆菌)的研究性文章。该研究成果为治疗多重耐药大肠杆菌感染带来了新希望,科研人员开发出一种仿生巨噬细胞 Fe3O4@PLGA 颗粒,该颗粒能在不伤害正常细胞的情况下高效杀灭多重耐药大肠杆菌,为解决耐药菌感染难题提供了新的思路。
多重耐药(MDR)大肠杆菌感染严重威胁全球公共健康,当前抗生素治疗手段在应对这类感染时面临诸多困境,新抗生素研发周期长,而细菌耐药性进化速度快,开发有效且安全的替代治疗策略迫在眉睫。
在此背景下,研究人员受到巨噬细胞选择性生物催化特性的启发,构建了由活巨噬细胞(MΦ)和 Fe3O4@PLGA 纳米颗粒组成的智能催化体系。巨噬细胞作为人体重要的先天免疫细胞,能通过生物催化过程产生活性氧(ROS)抵御微生物入侵,且对正常细胞和病原体具有选择性,不过其自身产生的 H2O2 浓度较低,抗菌活性有限。而 Fe3O4@PLGA 纳米颗粒中的氧化铁和 PLGA 均已获得美国食品药品监督管理局(FDA)批准,氧化铁纳米颗粒还具有类似酶的双重活性,能与 H2O2 在酸性环境中反应生成剧毒的羟基自由基(•OH),细菌感染的微环境恰好呈酸性。
实验结果显示,MΦ-Fe3O4@PLGA 颗粒对多重耐药大肠杆菌表现出优异的抗菌性能,体外抗菌效率高达 99.29%±0.31%。在与多重耐药大肠杆菌共培养后,该颗粒中的巨噬细胞会极化为 M1 型,释放 H2O2,同时产生脂滴(LD)。H2O2 与 Fe3O4@PLGA 反应生成•OH,而 LD 含有抗菌肽,可以靶向结合并杀灭细菌。
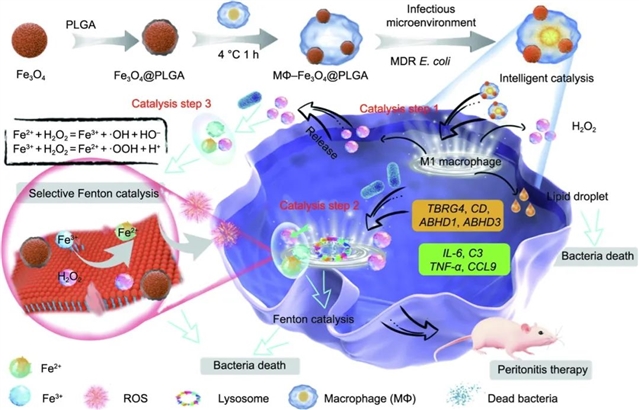
图 1. MΦ-Fe3O4@PLGA 颗粒的智能催化-治疗原理图。
通过 RNA 测序数据分析发现,这一过程激活了脂质代谢、多糖生物合成及代谢等相关途径。进一步研究表明,经过多次传代后,MΦ-Fe3O4@PLGA 颗粒的智能催化功能仍能部分保留。在体内实验中,该颗粒在感染部位能保持至少 6 小时,且可通过肝脏和肾脏代谢,对主要器官没有明显毒性,展现出良好的生物安全性。在腹膜炎模型实验中,MΦ-Fe3O4@PLGA 颗粒表现出较强的抗菌和治疗效果,能有效降低感染小鼠血液中的炎症细胞数量,减少主要器官中的细菌载量。
研究表明,MΦ-Fe3O4@PLGA 颗粒作为一种仿生智能催化剂,在治疗多重耐药大肠杆菌感染方面展现出巨大的潜力。虽然活细胞培养条件在一定程度上限制了其临床应用,但随着相关技术的发展,有望为耐药菌感染的治疗带来新的突破。
引用:
Jieni Fu, Xiangmei Liu, Zhaoyang Li, Yufeng Zheng, Yu Zhang, Hui Jiang, Yanqin Liang, Shengli Zhu, Zhenduo Cui, Shuilin Wu. Biomimetic Macrophage-Fe3O4@PLGA Particle-Triggered Intelligent Catalysis for Killing Multidrug-Resistant Escherichia coli. Engineering, 2024, 34(3): 174–186
开放获取论文:
https://doi.org/10.1016/j.eng.2023.05.022
更多内容
新技术助力探究M2巨噬细胞促进骨骼肌再生机制
福州大学团队开发新型抗菌纳米反应器为应对耐药菌威胁提供新路径
任其龙院士:MOF基材料高效分离过程研究进展
李骏院士等:智能网联汽车安全
Engineering征稿启事:人工智能赋能工程科技
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。