导读
脑科学研究的核心挑战之一在于解析复杂神经活动中多细胞类型(神经元、胶质细胞、血管内皮细胞等)的动态交互,尤其是神经血管耦合(Neurovascular Coupling, NVC)这一调控脑血流与代谢以匹配神经活动需求的关键生理过程。自1990年基于血氧水平依赖信号功能磁共振技术(BOLD-fMRI)问世以来,其凭借非侵入性、全脑覆盖的优势,成为探索脑功能与疾病机制的核心工具。然而,BOLD信号本质上是脑血流(CBF)、脑血氧(CBV)与氧消耗(CMRO2)变化的综合表征,且无法区分不同细胞类型(如神经元与星形胶质细胞)对信号的贡献。近日,同济大学物理科学与工程学院陈振跃教授联合苏黎世大学和苏黎世联邦理工学院Daniel Razansky教授团队提出一种突破性的混合成像平台—HyFMRI,通过融合基于光纤视镜的多通道光学成像模块和磁共振设备首次实现神经元、星形胶质细胞和血流反应的同步实时监测,为神经-胶质-血管相互作用提供了前所未有的研究视角。该技术已在小鼠模型中取得成功应用,为理解神经血管耦合机制和大脑功能研究打开了新局面。相关研究成果以 “Non-invasive large-scale imaging of concurrent neuronal, astrocytic, and hemodynamic activity with hybrid multiplexed fluorescence and magnetic resonance imaging (HyFMRI)” 为题发表于《Light: Science & Applications》。
研究背景
大脑是人体最复杂、最动态的器官,协调着支撑认知、感觉、运动和情感的多种功能。神经系统的每一次信号传递都是神经元、星形胶质细胞、周细胞、平滑肌细胞等多种细胞类型通过精密信号通路协同作用的结果。鉴于神经活动的高度复杂性和动态性,要深入理解大脑功能或病理,必须从不同细胞类型中记录多参数信号。然而,这一任务面临多重挑战:缺乏合适的对比机制、现有神经成像技术的性能限制,以及不同模态间的不兼容性。
基因编码钙指示剂可以实现神经元及其他细胞类型钙动态的可视化与量化,深刻改变了神经科学。与此同时,通过检测血氧水平依赖(BOLD)信号的功能性磁共振成像(fMRI)可以实现动物与人类全脑水平的功能与结构研究,但是却无法直接探测钙指示剂呈现的分子信息。为了实现这一目的,研究人员将光纤光度法钙成像与fMRI结合,实现了局部神经元活动与血流动力学的直接测量,为研究神经元-胶质细胞互作及更广泛的脑功能提供了有力工具。然而,光纤光度法缺乏空间分辨率且仅能探测小视野内细胞的平均信号。宽场荧光成像虽然可以绘制全皮层神经活动,却存在难以与fMRI整合的困境。
研究亮点
多模态光磁混合神经成像(HyFMRI)平台
本文提出了一种新型多模态光磁混合记录技术(HyFMRI)。成像平台集成9.4T磁共振系统、基于光纤镜的多通道宽场荧光与内源信号光学成像系统,和定制化表面射频线圈;通过3D打印组件连接两种模态,同时为实验动物提供生理保障(图1a)。多通道光学成像系统由磁共振兼容的光纤镜组成(包含10万根成像光纤和19根照明光纤),兼具荧光激发和探测,可同时对不同荧光标记(如GCaMP和RCaMP)神经细胞和光学内源信号成像(图1b-c)。该光纤镜的有效视场约为15毫米,空间分辨率约为70微米(图1d)。HyFMRI数据采集通过外部触发装置同步,可实现多模态数据采集与外部神经调制的精准时序匹配。
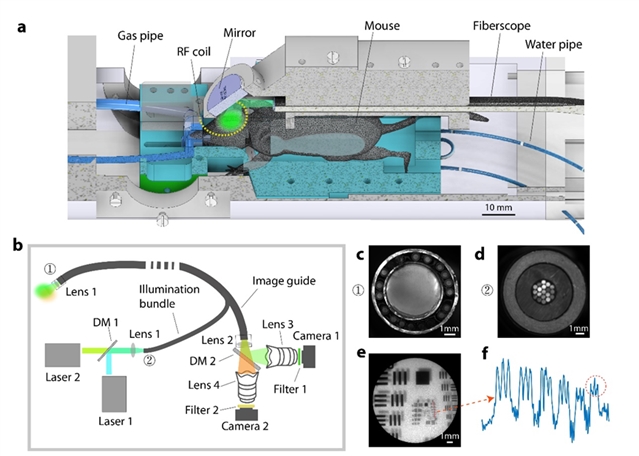
图1. 多模态荧光与磁共振成像(HyFMRI)平台。
多参量同步神经成像
基于HyFMRI成像平台,通过病毒转染钙指示剂实现星形胶质细胞(GCaMP6s)与神经元(RCaMP1.07)的标记,课题组研究了轻度麻醉状态下小鼠神经元、星形胶质细胞与血流动力学由电刺激诱发的大脑激活响应(图2)。HyFMRI成功捕获了对侧前肢初级体感皮层的神经活动-对应神经元激活强度(1.8908±0.1290%)、星形胶质细胞激活强度(1.9578±0.0780%),以及全皮层的血流动力学响应(1.3436±0.1609%)(图2a-c)。同侧半球未观察到明显激活。神经元激活动力学响应(达峰时间3.8357±0.5069 s,图2d)远快于星形胶质细胞(6.6714±0.3520 s,图2e)和BOLD信号(8.1111±0.5879 s,图2f),揭示了由神经元活动到血流动力学的传递过程。进一步分析显示,RCaMP/GCaMP的相关性(0.5281±0.0303)显著高于RCaMP/BOLD组(0.3769±0.0435,p=0.0115)和GCaMP/BOLD组(0.2959±0.0670,p=0.0061),揭示了钙信号与BOLD信号间存在的复杂非线性关系(图2g),同时也为星形胶质细胞参与神经血管耦合提供了直接证据。
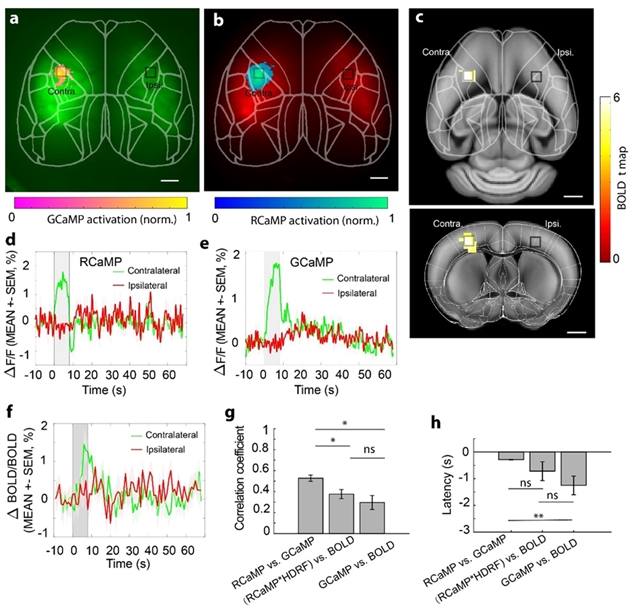
图2. 小鼠神经细胞类型特异的多参数大脑激活响应。
总结与展望
基于HyFMRI技术,团队成功同步测量了小鼠模型中神经元和星形胶质细胞的钙信号以及相应的血流变化。结果显示,电刺激诱发的神经元响应最快和激活强度最高,星形胶质细胞次之,BOLD最后。此外,神经元与星形胶质细胞的激活轨迹呈现高度线性相关,这为星形胶质细胞参与神经血管耦合提供了直接证据。
HyFMRI平台能够跨尺度、多参量监测复杂大脑活动,通过捕捉神经细胞相互作用和血流变化为研究大脑健康和疾病提供了新的途径,可广泛应用于神经退行性疾病、中风和认知障碍等基础研究和临床应用中。(来源:LightScienceApplications微信公众号)
相关论文信息:https://doi.org/10.1038/s41377-025-02003-9
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。