科技日报讯 (记者刘霞)英国曼彻斯特大学生物技术研究所(MIB)团队在5月7日出版的《自然·化学》杂志发表研究称:通过将光敏分子噻吨酮嵌入酶结构,他们研制出一系列特殊光驱动酶。这种酶可作为特殊催化剂,在可见光下即可工作,有望为药物和重要化学品生产带来更环保、高效的解决方案。
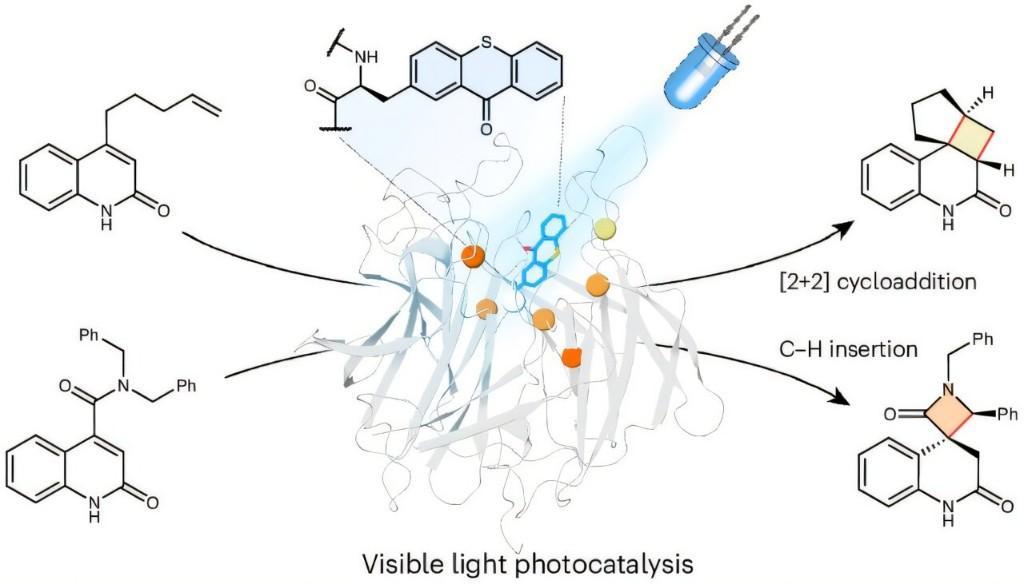 图片来源:《自然·化学》杂志
图片来源:《自然·化学》杂志
?
传统光驱动的化学过程存在明显短板,不仅要依赖有害的紫外线,还需使用可能产生副产物的化学光敏剂。这些光敏剂吸收光,将能量传递给其他分子以驱动化学反应。MIB团队曾尝试将紫外线光敏剂植入蛋白质,虽然提高了反应选择性,但仍面临光化学效率低、损伤分子、带来不必要副产物等问题。
为攻克这些难题,团队将噻吨酮嵌入酶中,获得多种新型光酶。新型光酶展现出三大优势:一是完全规避紫外线危害,因为噻吨酮能在可见光下工作;二是与工业照明条件完美匹配;三是反应速度和精准度显著提升。其中一种名为VEnT1.3的酶表现尤为突出,不仅能完成1300多次高效反应循环,还可精确调控分子的三维形状,这对确保药物有效性至关重要。
更令人振奋的是,这些光酶还开辟了前所未有的制造途径。以SpEnT1.3型酶为例,它能构建传统化学方法难以实现的螺旋环β-内酰胺结构,这类复杂的环状分子是众多药物的重要骨架。此外,这些工程酶展现出传统催化剂难以比拟的控制能力,能有效阻断有害中间产物的生成。
最新技术既可减少化学废弃物,又能降低能耗。随着遗传编码技术的进步,他们希望能设计出更多光酶,以前所未有的精度和效率驱动复杂化学反应,为制药、农用化学品、材料科学等诸多领域带来革命性变化。
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。