近日,大连理工大学宁波研究院解兆谦教授与美国西北大学John A. Rogers教授、俄勒冈大学Jonathan T. Reeder助理教授课题组合作,发明了一种生物可吸收的柔性微流控设备。其通过液体汽化冷却实现了对神经传导的阻滞,并且可以用于替代阿片类止痛药,达到无损伤的精准镇痛效果。相关研究成果发表于《科学》(Science)。
疼痛是临床中需要特别关注的问题之一。通过局部冷却形成可逆性神经阻滞,不仅可以达到按需消除疼痛的效果,而且能够完全避免服用阿片类药物以及其他镇痛剂所带来的副作用。传统的局部冷却技术需要借助大型医疗设备并在特定环境下实施,往往很难达到精准的冷却效果,在实际应用中存在着很大的局限性。
针对上述问题,研究团队设计了一种柔性、自缠绕(免缝合)、生物可吸收的周围神经冷却微流控设备,其能够在活体组织的任意深度提供精准、微创的冷却效果。该柔性设备集成了微流控系统与电路系统,通过控制该设备微流控系统中输入流体的流速与流量,并借助全氟戊烷液体的汽化吸热,实现了在特定部位提供精准且持续的冷却效果。而将具有蛇状形貌的镁线温度传感器分布在该设备末端,通过传感器电阻变化实时获得温度反馈,成功实现了对温度的精确监控。同时,具有预拉伸的多层结构力学设计使得该设备可以形成自卷曲结构,无需缝合便可紧密贴附至需要冷却的神经表面并可形成良好的力-热交界面。该设备完全由水溶性材料构成,可依据个性化需求在规定的时间段内溶解于皮下组织的生物流体中。这避免了额外的拆除手术给病人带来的痛苦,可以很好地满足患者在长时段内的镇痛需求,相比现有技术和产品具有显著优势。
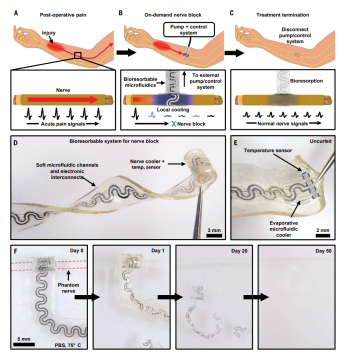
基于微流体、可精准阻滞神经的生物可吸收柔性冷却器(大连理工大学供图)
基于结构力学、传热学仿真分析,研究团队开展了结构和温控优化设计。该设备还实现了神经组织的精准无损冷却,有效阻滞了痛觉传导。
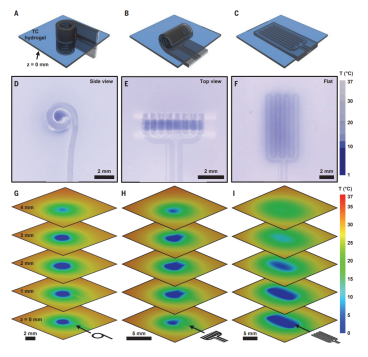
冷却区域的有限元模拟与实验(大连理工大学供图)
相关动物实验证实,该设备能在短时间内实现低温调控,并且能够很好地抑制神经活动。长期观察表明,复温后神经活动迅速恢复正常,且不会产生任何副作用。该设备同样可对自由活动的动物模型提供优异的按需镇痛效果。通过对动物模型进行相关组织学分析发现,该设备袖带在植入人体6个月后仍能与神经紧密接触,显示了极其优越的力学性能。同时,生物实验也验证了该设备具有很好的生物相容性与可吸收性。

冷却诱导神经阻滞和镇痛的实验情况(大连理工大学供图)
该工作首次展示了生物可吸收的植入式微型柔性冷却器在神经阻滞疼痛方面的成功应用,对未来基于柔性医学器件的疼痛管理研究具有非常重要的指导意义。
相关论文信息:https://www.science.org/doi/10.1126/science.abl8532
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。