2026年4月29日,美国埃默里大学梁波团队在Nature Communications发表题为“Orchestrated and dynamic nucleotide addition cycle during respiratory syncytial virus early-stage elongation”的研究论文。该研究利用冷冻电镜单颗粒技术,捕捉了呼吸道合胞病毒聚合酶在早期RNA延伸过程中的多个关键构象状态,系统揭示了RSV聚合酶在核苷酸添加循环中的动态构象变化与催化机制。研究还首次在NTP结合状态和转位后状态中观察到RSV聚合酶L蛋白全部五个结构域的结构,为理解单负链RNA病毒RNA合成机制,以及开发靶向病毒聚合酶的抗病毒药物提供了重要结构基础。
呼吸道合胞病毒(Respiratory Syncytial Virus,RSV)是一种高度传染性的人类病原体。婴幼儿、老年人、免疫功能受损人群以及心肺疾病患者均是RSV感染的高危人群。RSV属于肺病毒科(Pneumoviridae)单负链RNA病毒,其基因组为单链负义RNA。RSV的RNA转录和复制由RNA依赖性RNA聚合酶(RNA-dependent RNA polymerase,RdRP)催化完成。该聚合酶复合物由多功能聚合酶蛋白L(Large protein)和辅助因子磷蛋白P(Phosphoprotein)组成。其中,L蛋白包括五个结构域:RNA依赖性RNA聚合酶结构域(RdRp)、加帽结构域(Cap)、连接结构域(CD)、甲基转移酶结构域(MT)和C末端结构域(CTD)。P蛋白则主要包括N端结构域(PNTD)、寡聚化结构域(POD)和C端结构域(PCTD)(图1a)。
RSV的RNA合成过程包括起始、延伸和终止三个阶段。在RNA延伸过程中,聚合酶通过不断重复核苷酸添加循环,逐步延长新生RNA产物链。一个典型的核苷酸添加循环通常包括四个主要步骤:首先,新的核苷三磷酸进入聚合酶活性中心,并与模板RNA的+1位点碱基配对;随后,活性位点闭合,使RNA模板、RNA产物、核苷酸、催化金属离子和聚合酶处于适合催化的位置;接着,新的磷酸二酯键形成,并伴随焦磷酸释放;最后,RNA模板-产物双链向前转位一个碱基对,使+1位点重新空出,为下一轮核苷酸添加做好准备。
此前,梁波团队已经解析了启动子RNA结合状态下的RSV聚合酶结构,揭示了RSV RNA合成起始阶段的结构基础。然而,在RNA延伸过程中,聚合酶如何招募新的核苷三磷酸、如何完成磷酸二酯键形成,以及如何推动RNA模板-产物双链向前转位,仍缺乏直接的结构证据。尤其是,RSV聚合酶L蛋白中的CD、MT和CTD结构域在以往解析的apo状态和启动子结合状态中高度柔性,未能被解析,其在RNA合成过程中的结构状态和功能作用仍不明确。
在本研究中,为捕捉RSV聚合酶在延伸过程中的不同构象状态,作者设计了一种发夹状RNA模拟物Tr3-mimic,以提高RNA模板与引物之间的配对效率(图1b)。随后,作者将RSV聚合酶分别与不同RNA底物、核苷酸或核苷酸类似物组装,并通过冷冻电镜解析了早期RNA延伸过程中的四种核苷酸添加循环关键状态:NTP结合状态、反应前状态、转位前状态和转位后状态(图1c)。其中,NTP结合状态和转位后状态的结构显示出L蛋白全部五个结构域;而反应前状态和转位前状态与apo状态及启动子结合状态相似,仅能解析L蛋白中的RdRp和Cap两个结构域。
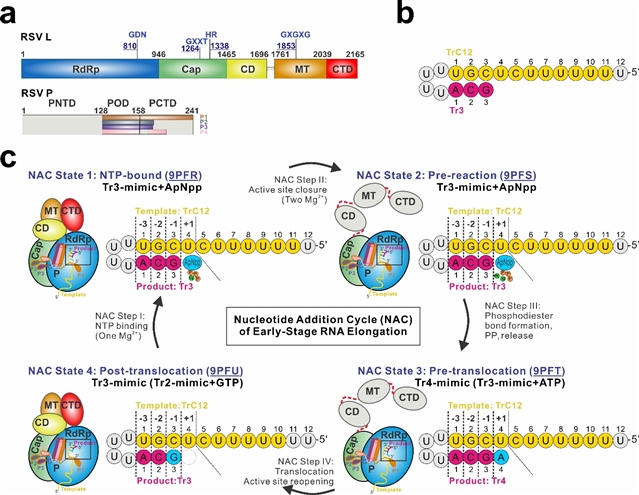
图1:RSV聚合酶结构组成、Tr3-mimic RNA设计及早期RNA延伸过程中四种核苷酸添加循环关键状态的转换示意图
将RSV聚合酶与TrC3-mimic和ApNpp在室温下孵育后,作者获得了分辨率为3.08 Å的NTP结合状态冷冻电镜结构。该结构包括L蛋白的五个结构域,以及P蛋白的POD和PCTD结构域(图2a-b)。高分辨率冷冻电镜密度图显示出清晰的RNA双链、核苷酸类似物ApNpp,以及一个位于催化残基D700、D811和ApNpp之间的镁离子(图2c)。结构分析显示,RdRp和Cap结构域共同形成类似“碗状”的催化核心,而在apo状态和启动子结合状态下高度柔性的CD、MT和CTD结构域则位于该“碗状”结构上方(图2d)。CD-MT-CTD模块与RdRp-Cap模块之间的相互作用整体较弱,主要由supporting helix和supporting loops等局部结构元件介导(图2e-h)。
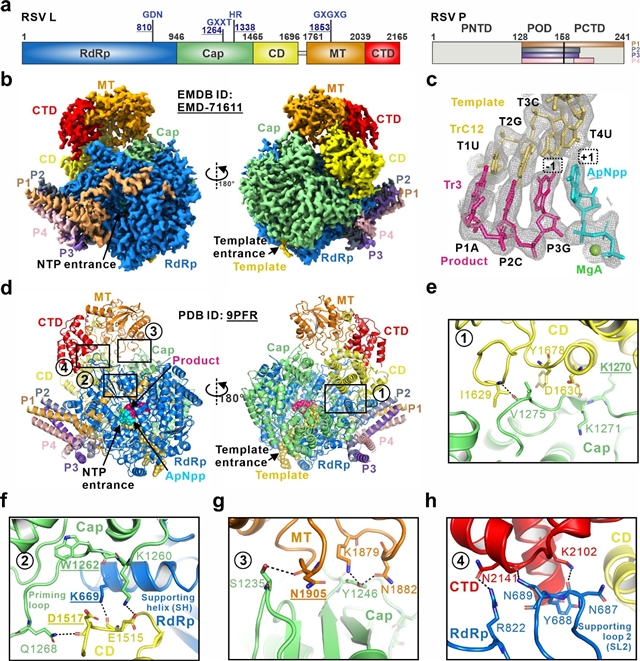
图2:RSV聚合酶NTP结合状态结构,以及五结构域L蛋白中RdRp-Cap模块与CD-MT-CTD模块之间的相互作用
进一步比较apo状态、启动子结合状态以及四种RNA延伸状态后,作者发现RSV聚合酶在RNA合成过程中的构象变化可分为两个层面。第一个层面是宏观结构域重排,主要表现为与supporting helix和supporting loops相关的CD、MT和CTD结构域在不同状态中的有序化和无序化。第二个层面是活性中心附近保守微观motif的精细构象调整,包括motif A、motif C、motif D和motif F在不同催化状态中的动态变化。
其中,supporting helix和supporting loops在不同状态中呈现“开放”和“闭合”两种构象,与CD-MT-CTD模块的稳定性及构象变化密切相关。启动子RNA结合可诱导motif F发生构象变化,其保守氨基酸残基K619参与稳定+1位点的模板核苷酸。在apo状态和启动子结合状态中,含有催化位点GDN的motif C呈伸展状态,motif A也靠近催化位点;而在RNA延伸状态中,motif C发生弯曲,motif A向外移动,从而为RNA产物链和新进入的核苷酸提供空间。同时,motif D中的K856在NTP结合状态和反应前状态中靠近核苷酸的三磷酸基团,而在催化完成后远离活性中心。
这些结果表明,RSV聚合酶在RNA延伸过程中并不是简单重复化学反应,而是通过多结构域、多保守motif、RNA底物、核苷酸和金属离子之间的动态协同调控,连续完成RNA模板识别、核苷酸选择、磷酸二酯键形成和RNA转位等关键步骤。
综上所述,该研究首次系统捕捉了RSV聚合酶在早期RNA延伸过程中的四个关键核苷酸添加循环状态,揭示了RNA模板、RNA产物、核苷酸、镁离子以及聚合酶保守motif之间的动态协同关系。该研究不仅补全了RSV聚合酶从RNA合成起始到早期延伸阶段的重要结构图景,也为理解单负链RNA病毒聚合酶的共性机制和病毒特异性调控提供了重要依据。由于RSV聚合酶是抗病毒药物开发的重要靶点,这些结构发现也为开发靶向RSV及相关病毒聚合酶的广谱抗病毒策略提供了新的结构基础,相关病毒包括狂犬病毒、尼帕病毒和埃博拉病毒等。
文章通讯作者为梁波博士。梁波博士本科毕业于中国科学技术大学,博士毕业于佛罗里达州立大学,随后在哈佛医学院开展博士后研究,现为美国埃默里大学副教授。梁波实验室主要结合冷冻电镜、晶体学和生物化学方法,研究生物大分子的结构与功能机制,研究方向包括单负链RNA病毒RNA合成机制以及神经生物学疾病相关蛋白质的折叠机制。团队目前正在招聘博士后,欢迎感兴趣的学生联系梁波实验室(https://med.emory.edu/departments/biochemistry/research-labs/liang/index.html);
文章第一作者为曹冬冬博士,现为美国埃默里大学梁波团队副研究员。曹冬冬博士本科毕业于中国科学技术大学,并于中国科学技术大学获得博士学位。(来源:科学网)
相关论文信息:https://www.nature.com/articles/s41467-026-72519-0
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。