|
|
|
|
|
运动营养中的硒与骨骼肌健康| MDPI Nutrients |
|
|
论文标题:Selenium and Skeletal Muscle Health in Sports Nutrition
论文链接:https://www.mdpi.com/2072-6643/17/11/1902
期刊名:Nutrients
期刊主页:https://www.mdpi.com/journal/nutrients
前言
硒主要通过硒蛋白在体内发挥功能,硒蛋白是一类含有第21种氨基酸——硒半胱氨酸(Sec)的特殊蛋白质家族。Sec由UGA终止密码子编码,其正确插入需要mRNA 3端非翻译区中的SECIS元件及SBP2蛋白的协同作用。目前人类已发现25种硒蛋白,它们参与调节甲状腺激素代谢、细胞内外的抗氧化反应、内质网蛋白反向运输等关键生物学过程,对维持细胞和组织稳态至关重要。硒缺乏会导致多种疾病,其中骨骼肌是主要靶器官。硒缺乏可引起肌肉收缩功能受损、坏死和萎缩,并影响卫星细胞介导的肌肉再生能力。本文从三个方面综述硒与硒蛋白在维持骨骼肌健康中的机制:(1)抗氧化调节;(2)线粒体功能调控;(3)蛋白质代谢调节,并探讨其在提升运动表现和延缓肌肉衰老中的实际应用前景。
骨骼肌生物学中的硒蛋白
硒在哺乳动物中主要通过硒蛋白发挥生理功能。目前已知的25种硒蛋白中,GPX4和TXNRD2定位于线粒体,DIO2、SELENOK、SELENOS等7种位于内质网,共同调控细胞器稳态。研究表明,多种硒蛋白通过协同作用参与骨骼肌健康维持:SELENOW通过RAC1-mTOR通路调节蛋白质代谢与钙稳态;SELENON和SELENOK调控内质网钙释放与应激反应,影响肌细胞分化与再生;GPx和Txnrd家族是关键的抗氧化酶,清除ROS并抑制脂质过氧化;SELENOT、SELENOS等通过调节内质网蛋白降解、氧化还原平衡和线粒体功能,共同抵抗肌肉萎缩、肌营养不良和衰老性肌少症。硒缺乏会导致这些蛋白表达下降,破坏细胞内稳态,进而引发肌肉病变。当前研究仍需深入揭示硒蛋白网络在肌肉疾病中的协同机制(图 1)。
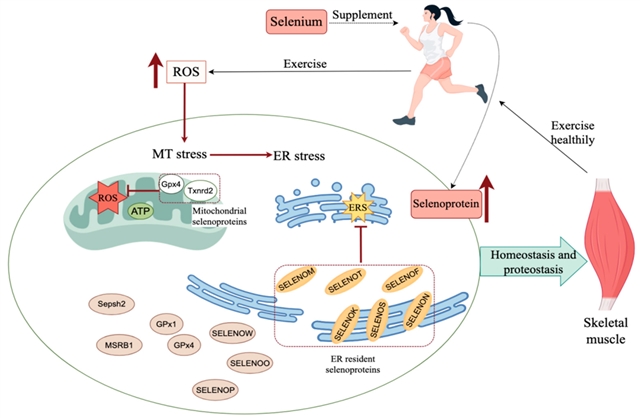
图 1 硒蛋白网络通过协同抗氧化和缓解内质网/线粒体应激提升运动耐力
硒在肌肉健康中的作用机制
硒是维持哺乳动物骨骼肌健康的关键微量元素,主要通过硒蛋白发挥作用。骨骼肌占体重的30–40%,具有运动、产热和保护等重要功能。运动诱导的氧化应激会破坏线粒体功能,导致ROS过量产生,打破氧化还原平衡,抑制合成代谢并加速分解代谢,最终引起肌肉流失。适量补硒可通过以下机制改善肌肉功能:(1)增强GPx等抗氧化酶的活性,减轻氧化损伤;(2)调节SELENOT、SELENON等线粒体功能相关硒蛋白,维持能量代谢和ATP生成;(3)通过SELENOW-RAC1-mTOR等通路协调蛋白质合成与降解平衡,防止肌肉萎缩;(4)参与钙稳态调控,影响STIM1/TRPC1等钙通道功能,促进肌细胞分化与再生。因此,硒及其硒蛋白在抗氧化、能量代谢、蛋白平衡和钙信号等多个层面共同维持骨骼肌稳态。
硒缺乏与肌肉病变
硒缺乏会损害骨骼肌的最大收缩强度和等速扭矩,导致姿势不稳定和运动功能障碍,并伴有血清肌酸激酶和乳酸脱氢酶活性降低,临床表现为肌肉疼痛和疲劳。它是人类多种心肌和骨骼肌疾病的诱因,例如以心肌坏死、炎症浸润和钙化为特征的克山病,其机制与硒缺乏削弱GPx等硒酶活性、破坏氧化还原稳态并加剧病毒基因组损伤有关。此外,硒缺乏也与肌少症密切相关;低血浆硒水平易导致髋部力量和握力下降,而补硒可通过保护运动神经元功能和减少神经肌肉接头退化,延缓肌肉萎缩的进程。
运动与骨骼肌适应
高强度运动会诱发肌肉损伤,导致延迟性酸痛和肌力下降,其机制涉及收缩蛋白结构破坏、钙调控紊乱及活性氧(ROS)过度产生。补充硒可能通过增强硒蛋白(如GPx)的抗氧化活性,减轻运动引起的氧化损伤和脂质过氧化,从而有助于运动恢复和机能改善。然而,硒的效果受其剂量和形态影响:有机硒(如硒代蛋氨酸、纳米硒)的生物利用度优于无机硒,但过量摄入可能引发硒中毒。目前虽有一些研究表明硒能提升机体抗氧化能力,尤其在与抗阻训练结合时效果更佳,但最佳补充剂量、时机及形态仍需进一步研究确定。
临床意义和未来方向
针对硒蛋白的干预策略中,SELENOP作为兼具生物标志物和转运功能的关键蛋白,其表达受膳食硒、炎症及缺氧等多种因素调控。目前治疗肌肉疾病缺乏靶向递送系统,但纳米技术(如钙整合纳米颗粒)的发展为组织特异性调控提供了新途径,硒纳米干预未来可能用于肌肉疾病治疗。硒与维生素E在抗氧化中具有协同作用:两者同时缺乏可诱发严重肌病,而联合补充能显著提升GPx和SOD活性,降低运动后MDA和LDH水平,改善机体抗氧化状态。此外,肠道-肌肉轴可能介导硒对骨骼肌的调节作用,肠道菌群通过代谢通路和线粒体动力学(如DRP1调控的线粒体分裂)影响肌肉功能与运动能力,提示硒的补充效果可能与肠道微生态密切相关。
总结
硒通过抗氧化防御、精准调控硒蛋白合成及协调氧化还原信号通路三大机制,维持骨骼肌稳态并提升运动能力。现有研究多基于动物模型,亟需临床试验验证因果关系。未来应聚焦于:剂量反应优化、硒蛋白-肌肉互作网络的系统阐释,以及通过随机对照试验验证硒的运动增益潜力,以推动其在运动营养和预防医学中的精准应用。
Nutrients 期刊介绍
主编:
Maria Luz Fernandez, University of Connecticut, USA;
Lluis Serra-Majem, University of Las Palmas de Gran Canaria, Spain
期刊主题涵盖常量营养素、微量营养素、生物活性营养素、运动营养、公共卫生和饮食相关疾病等学科领域。
|
2024 Impact Factor
|
5.0
|
|
2024 CiteScore
|
9.1
|
|
Time to First Decision
|
12.9 Days
|
|
Acceptance to Publication
|
2.3 Days
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。