导读
传统光固化3D打印技术虽然能够实现高精度制造,但在生物组织等强散射介质中的应用却面临巨大的挑战——难以穿透如生物组织这样的强散射介质,光线会被打散成杂乱无章的光斑,无法聚焦。同时,常用的紫外/蓝光穿透力弱,限制了其在深部组织或高密度细胞结构中的应用。
近日,来自瑞士洛桑联邦理工学院的研究人员独辟蹊径,巧妙利用上转换纳米粒子(UCNPs) 和智能光场调控技术,首次成功在300μm厚的强散射介质(如鸡胸肉)后方实现了微米级分辨率的非侵入式光固化打印,如图1所示。这项技术为无创或微创生物打印、靶向药物递送和组织工程开辟了激动人心的全新路径。
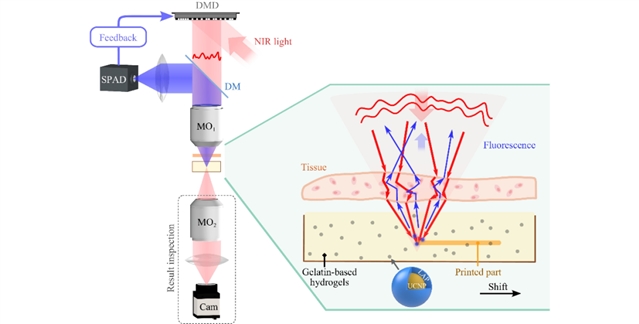
图1:使用涂有光引发剂LAP的UCNP进行高分辨率非侵入性增材制造的示意图
穿透散射介质的光学机制与材料创新
传统用于光固化的紫外或蓝光(能量高但穿透浅)进入后会被强烈散射和吸收,导致光斑扩散、能量分散,无法实现高精度打印。而近红外光(NIR)凭借更长的波长,在生物组织中的散射相对较弱,且处于“光学治疗窗口”,吸收少、穿透更深,是深入体内的理想“能量快递员”。然而,NIR本身能量不足以直接引发常见光敏材料(光引发剂)的聚合反应。对此,研究团队合成的UCNPs具备一项神奇能力:它们能吸收多个低能量的NIR光子,将其“上转换”成单个高能量的紫外(UV)光子和可见光光子。UV光子负责激发光引发剂(LAP),触发周围水凝胶单体(gelMA)的光聚合反应,实现结构固化。而可见光光子则扮演了至关重要的“导星(Guide Star)”角色,为后续的光场调控提供反馈信号。这种利用NIR激发UCNPs产生UV进行聚合的策略,巧妙地绕过了传统短波长光穿透力差的根本限制。
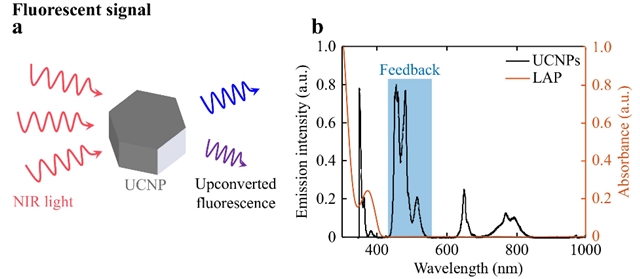
图2:上变频过程的示意图与在976 nm光照射下UCNPs的发射光谱(黑色)和光引发剂LAP的吸收光谱(橙色)
基于反馈优化的智能光场调控
即使有了穿透力强的NIR和产生UV的UCNPs,散射效应依然会使光线在组织中形成散斑,破坏聚焦效果。研究团队构建了一套精密的自反馈非侵入式打印系统。NIR首先通过一个高速数字微镜器件(DMD)进行空间光调制,调制后的光穿过散射介质(鸡胸组织或全息扩散片)照射到含有UCNPs和光引发剂的水凝胶树脂上。UCNPs被激发产生的可见光“导星”荧光会部分反向散射回来,被一个高灵敏度的单光子雪崩二极管(SPAD) 探测器捕获。这个看似微弱的反向散射荧光信号,蕴含了光穿过散射介质后内部光场分布的关键信息。关键在于利用这个荧光信号作为反馈进行迭代优化。团队采用了一种称为可分离自然进化策略(SNES) 的智能算法。算法不断尝试不同的DMD调制图案,目标是最大化一个经过功率校正的“适应度函数”。经过数百次迭代,算法最终能找到最优的DMD图案,补偿散射带来的波前畸变,在树脂内部形成一个接近衍射极限(约1.65μm)的明亮聚焦光斑。整个过程无需在样品后方放置探测器,真正实现了非侵入式聚焦。
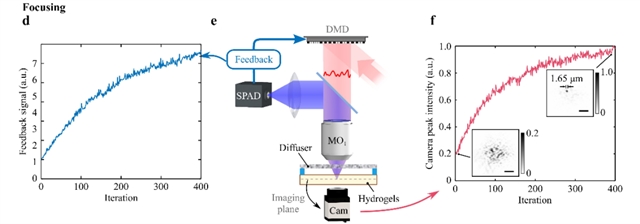
图2:基于非线性荧光反馈的聚焦过程
光学记忆效应驱动动态扫描打印
要打印复杂结构,需要能够快速、精确地在三维空间内移动激光焦点。研究团队巧妙地利用了光在散射介质中的传播会保留一定的相关性,通过这一特性可以优化聚焦过程。在生物组织中,这种平移相关的记忆效应范围相对有限(本研究中鸡胸组织的平移记忆效应半高宽约8μm)。基于此,团队开发了“动态聚焦扫描(Dynamic Focusing and Scanning)” 策略。在目标区域的起点,使用上述反馈优化获得一个最佳聚焦点。保持当前优化的DMD图案不变,横向平移样品(利用记忆效应等效于移动焦点)。焦点会跟随移动,但强度会随移动距离增加而衰减,对比度也会下降。当移动距离接近记忆效应范围(例如每移动5μm)时,停止扫描。将上一个优化点获得的DMD图案作为初始猜测,再次启动快速优化(约20秒)。由于起点接近全局最优解,此次优化收敛速度大大加快。重复上述步骤,结合高功率扫描(触发聚合)和低功率聚焦优化(利用非线性加速),像“接力”一样,逐步构建出整个设计结构。
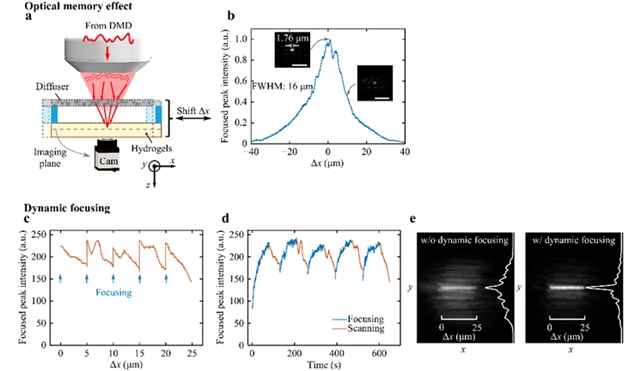
图3:动态扫描策略示意图与实际效果对比
通过此策略,研究团队穿过300μm厚的鸡胸组织,成功打印出清晰可辨的微米级字母结构(如“EPFL”),特征尺寸约2μm,最小可分辨间距达2μm。在仅使用同侧(入射光侧)探测器的情况下,成功通过散射介质(全息扩散片)打印出精细线条(特征尺寸1.78 ± 0.39 μm)和小于散斑尺寸的字母“E”,证明了技术的非侵入核心能力。
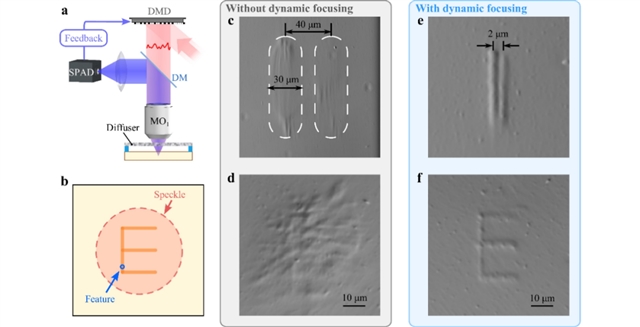
图4:非侵入式打印的实验设置与实际打印效果对比
总结与展望
EPFL团队这项研究首次将上转换纳米粒子、基于非线性反馈的非侵入式波前整形以及光学记忆效应驱动的动态聚焦扫描三大核心技术完美融合,在强散射生物组织后方实现了真正的微米级分辨率非侵入式光固化3D打印。这项技术不仅将推动无创体内生物打印的前沿,还为未来个性化医疗、器官再生等领域的应用开辟了新的可能性。
展望未来,这项非侵入式打印技术仍有提升空间。当前聚焦优化时间(几十秒)对于动态的生物组织(变化时间尺度在毫秒级)而言较慢,通过开发更灵敏探测器、更高效率UCNPs、更快速鲁棒算法以及更高速光调制器可以实现更高速的加工效率。在加工定位方面,“盲聚焦”特性导致焦点起始位置随机,未来需结合具有空间分辨能力的反馈定位技术,实现对打印体素绝对位置的精确控制,这对复杂结构至关重要。(来源:先进制造微信公众号)
相关论文信息:https://doi.org/10.37188/lam.2025.021
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。