|
|
|
|
|
苦木素类化合物抗癌研究新进展:天然产物的抗癌潜力再受关注 Engineering |
|
|
论文标题: The Anticancer Potential of Quassinoids—A Mini-Review
期刊:Engineering
DOI:https://doi.org/10.1016/j.eng.2023.11.022
微信链接:点击此处阅读微信文章
《Engineering》发表了一篇题为“The Anticancer Potential of Quassinoids—A Mini-Review”(苦木素类化合物的抗癌活性研究)的综述文章。该研究由南京中医药大学和美国伊利诺伊大学芝加哥分校的研究团队共同完成,系统总结了苦木素类化合物在抗癌领域的最新研究进展,包括其细胞毒性、抗肿瘤活性、作用机制、安全性评价以及与临床抗癌药物联合使用的潜在益处。陆彩为文章第一作者,赵明、车镇涛为通讯作者。

癌症是全球第二大死亡原因,占死亡病例的四分之一。随着人口增长和老龄化,癌症预计将成为本世纪的主要死亡原因之一。目前,手术结合化疗或放疗是大多数癌症患者的一线治疗手段,但这些治疗手段往往伴随着严重的副作用和生活质量下降。因此,寻找新的、有效的抗癌策略至关重要。天然产物,尤其是植物代谢物,一直是抗癌药物的重要来源。苦木素类化合物是一类仅在苦木科植物中发现的高度氧化和降三萜内酯,具有广泛的生物活性,包括细胞毒性和抗肿瘤特性。
研究表明,苦木素类化合物对多种癌细胞表现出显著的细胞毒性。例如,鸦胆子苦醇对非小细胞肺癌细胞的半数抑制浓度(IC50)值低至0.028 μmol/L,显示出与紫杉醇相当的细胞毒性效力。此外,鸦胆子素A对胰腺癌细胞的选择性抑制作用高于其他肿瘤类型,其IC50值仅为29 nmol/L。这些化合物不仅在体外表现出强大的细胞毒性,还在动物模型中显示出显著的抗肿瘤特性。例如,在小鼠原位胰腺癌模型中,鸦胆子素D的抗肿瘤效果与吉西他滨相当。
苦木素类化合物的细胞毒性机制主要涉及细胞凋亡、细胞周期阻滞和上皮-间质转化(EMT)程序的参与。细胞凋亡通过内源性(线粒体介导)和外源性(死亡受体介导)两条通路实现。例如,鸦胆子素D通过激活线粒体介导的通路诱导癌细胞凋亡,而宽缨酮则通过抑制AKT/NF-κB信号通路激活外源性凋亡。此外,苦木素类化合物还能通过抑制PI3K/AKT/NF-κB等信号通路,阻滞细胞周期于G0/G1期,从而抑制肿瘤细胞的增殖。
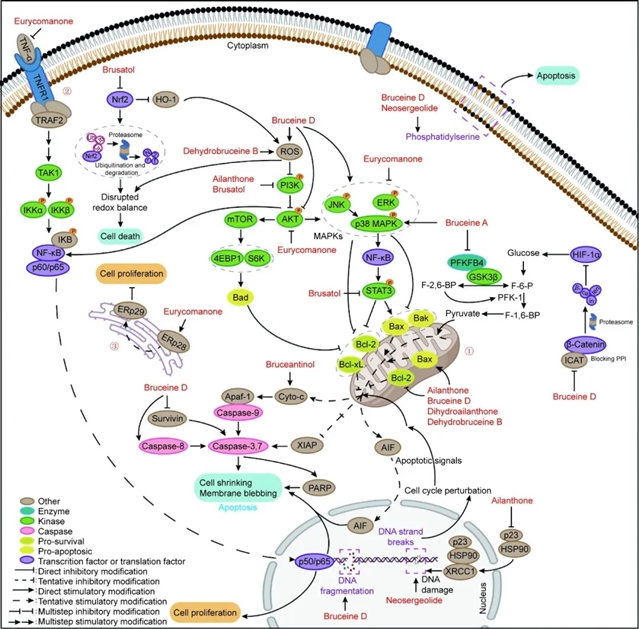
图1 苦木素诱导细胞凋亡的机制。
安全性评估显示,苦木素类化合物对正常细胞的毒性较低。例如,鸦胆子素D对正常人胃上皮细胞的IC50值高于487.33 μmol/L,远高于其对肿瘤细胞的毒性。此外,在动物实验中,苦胆子苦醇、鸦胆子素D等化合物在治疗剂量下未显示出明显的器官毒性。
更令人关注的是,苦木素类化合物与临床抗癌药物联合使用时,表现出显著的协同作用。例如,鸦胆子苦醇与顺铂联合使用,显著增强了对肺癌细胞的细胞毒性;与吉西他滨联合使用时,对胰腺癌细胞的抑制效果优于单独使用。此外,鸦胆子苦醇通过抑制Nrf2介导的抗氧化反应,增强了多种化疗药物的疗效。
苦木素类化合物在抗癌领域展现出巨大的潜力。其细胞毒性、抗肿瘤活性以及与临床抗癌药物的协同作用,使其成为未来抗癌药物开发的重要候选。未来的研究将进一步探索其作用机制,并通过化学修饰优化其药理特性,以开发出更具活性且毒性更低的类似物。
论文信息:
Cai Lu, Si-Nan Lu, Di Di, Wei-Wei Tao, Lu Fan, Jin-Ao Duan, Ming Zhao, Chun-Tao Che. The Anticancer Potential of Quassinoids-A Mini-Review. Engineering, 2024, 38(7): 27–38
开放获取:
https://doi.org/10.1016/j.eng.2023.11.022
更多内容
Engineering 2024年7月刊目录 | 天然药物专题
天然产物改善微循环障碍研究取得进展,为相关疾病治疗提供新方向
欢迎投票:2025全球十大工程成就评选
工业废水变宝!清华大学团队以创新电化学技术高效回收金属
Engineering征稿启事:人工智能赋能工程科技
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。