2021年11月29日,北京航空航天大学的王雪林团队、陈军歌团队与清华大学刘静教授团队合作在Matter上发表了一篇题为“Endosomal escapable cryo-treatment-driven membrane-encapsulated Ga liquid-metal transformer to facilitate intracellular therapy”的研究论文。
研究团队首次通过引入肿瘤细胞的细胞膜包裹Ga颗粒,实现了在冷冻条件下Ga颗粒变形,发生形变的Ga颗粒可在细胞内部刺破溶酶体,从而实现溶酶体逃逸,由此实现细胞内治疗并达到高效杀伤肿瘤的目的。
王雪林博士为论文第一作者,陈军歌博士与刘静教授共同担任论文通讯作者,北京航空航天大学为论文第一完成单位。
由于具有极佳的导电/导热性以及良好的机械性能和生物相容性,镓基液态金属(Ga-LM)材料近年来在许多领域都取得显著进展,如柔性电子、健康监护、人工骨替代物、体内成像和肿瘤治疗等。电、磁、光、热、化学等外部刺激能使LM发生剧烈形变。比如,电刺激能够使LM从原来的扁平状变为球形;大面积LM复合材料受热作用时会显示出从二维到三维形状的可控变化;电化学刺激可使LM在液滴和非对称结构之间发生大尺度可逆变形;在LM中掺入磁性铁颗粒后CuSO4等化学溶液可以引起LM表面张力的变化,导致LM产生不同的形变。总体而言,LM大尺度变形特性已在许多领域做出独特贡献,包括软体机器人、智能材料、仿生变形器等。与大尺度LM变形相比,微/纳米尺度的LM颗粒,需要在电子显微镜等工具的辅助下才能观察到其表面形貌,且小尺寸颗粒使得外部刺激场的精准施加极其困难,调控其变形具有极大挑战性,尤其在经过各种修饰后更是如此。
在此次报道的工作中,联合团队首次引入细胞膜包裹修饰的Ga颗粒(cell membrane-coated Ga Particles,Ga/MPs),该颗粒通过肿瘤细胞膜的归巢效应靶向肿瘤细胞,并通过胞吞作用进入到细胞的溶酶体内,在冷冻条件下发生剧烈形变,由原本的球形变成类似于仙人掌外形的刺突形,进而刺破溶酶体,从而实现Ga颗粒冷冻变形下的细胞内治疗(图1),这一策略极大提高了肿瘤冷冻治疗的精准性及效率。

图1:低温刺激包膜Ga颗粒变形实现溶酶体逃逸原理图。
研究中,借助低温透射电镜(Cryo-TEM)观察发现,在低温环境下Ga/MPs从球形结构向仙人掌状结构发生显著的形态转变(图2),直接穿透溶酶体膜(图3),从而达到杀伤细胞的目的。
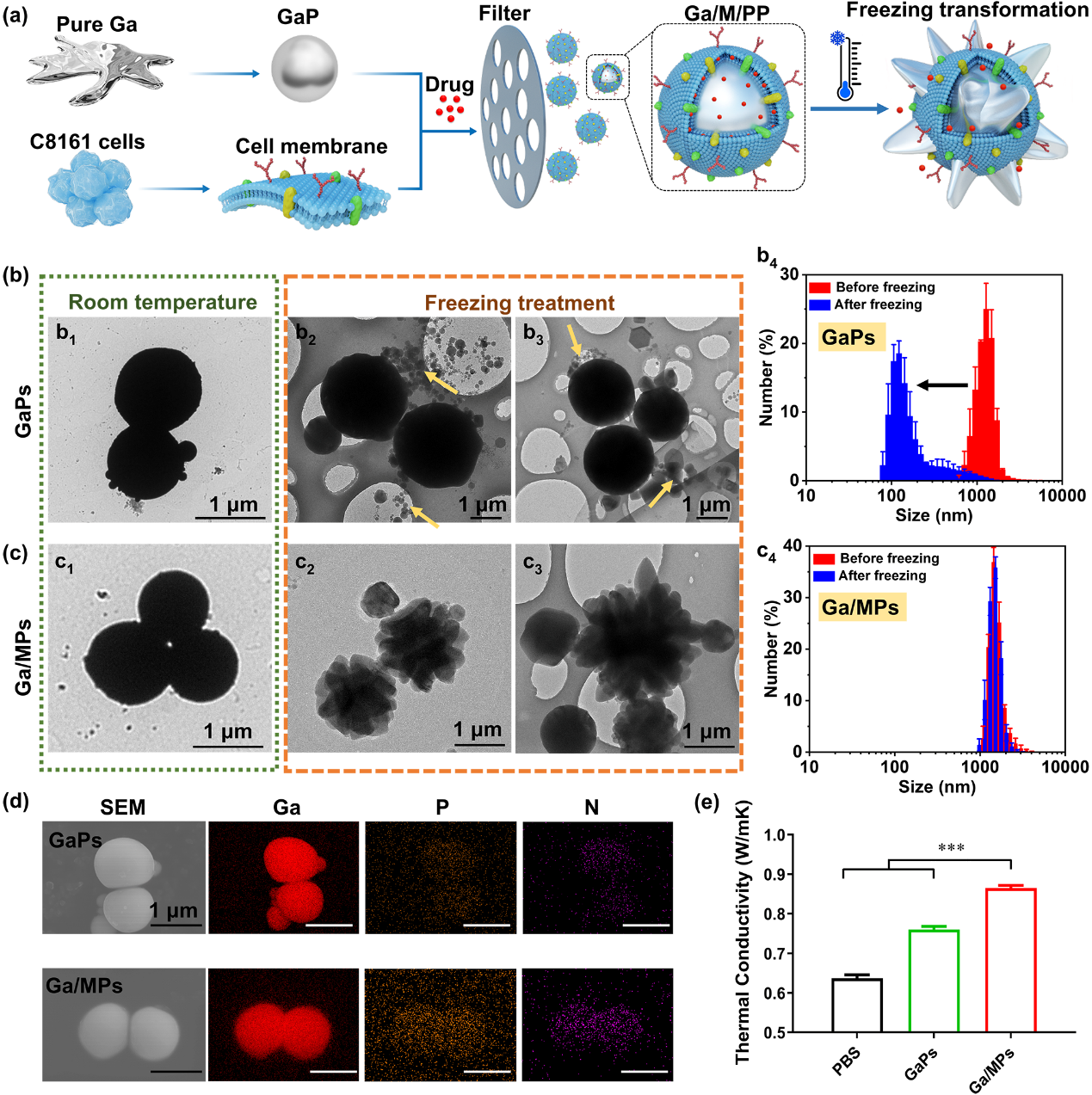
图2:Ga颗粒(GaPs)材料的制备与表征。(a) Ga/M/PP的制备及冷冻变形过程。(b) GaPs的TEM成像:(b1)室温下的TEM成像;(b2)和(b3) -196 ℃冷冻处理下的Cryo-TEM成像;(b4)动态光散射测试冷冻处理前后Ga颗粒的粒径。(c) Ga/MPs的TEM成像:(c1) 室温下的TEM成像;(c2)和(c3) Ga/MPs在-196 ℃冷冻处理下的Cryo-TEM成像;(c4)动态光散射测试冷冻处理前后Ga/MPs的粒径。(d) GaPs和Ga/MPs的SEM成像和EDS图谱。(e) PBS、GaPs和Ga/MPs的导热系数。
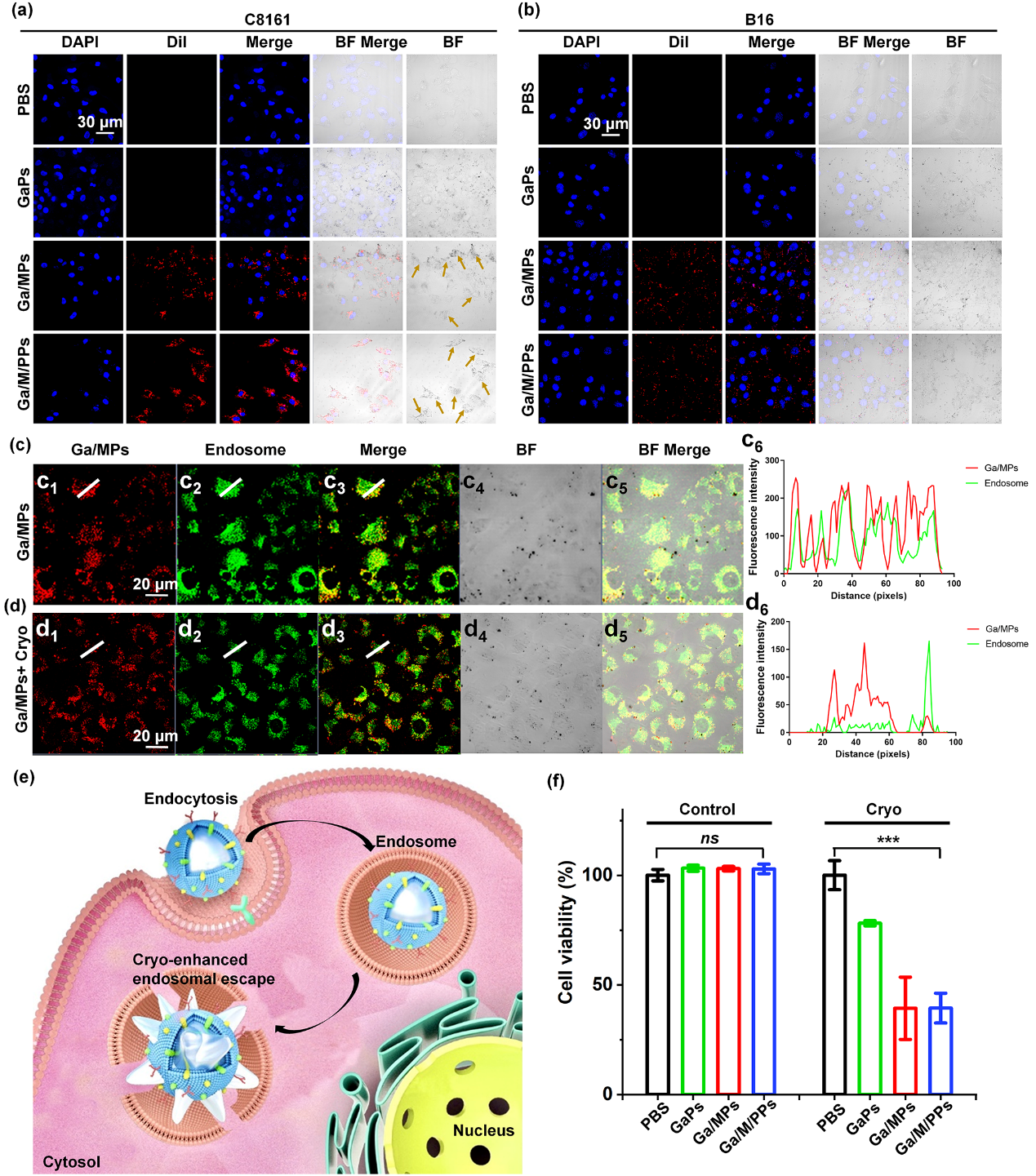
图3:Ga颗粒变形实现溶酶体逃逸。(a)和(b)三种Ga颗粒在细胞内的摄取情况。(c) Ga/MPs在人黑色素瘤C8161细胞中和溶酶体的共定位情况。(d)低温处理后Ga/MPs在人黑色素瘤C8161细胞中和溶酶体的共定位情况。(e)由Ga/MPs在低温处理下对溶酶体的机械破坏引起溶酶体逃逸示意图。(f)三种Ga颗粒的细胞毒性测试。
此外,Ga/MPs可携带抗肿瘤药物紫杉醇,在冷冻刺激下通过破坏溶酶体而释放,由此实现了高效的药物传递。在肿瘤部位注射携带紫杉醇的Ga/MPs后,颗粒通过胞吞进入溶酶体,低温处理可使该颗粒外表面产生刺突,刺穿溶酶体膜,从而使溶酶体内的水解酶和包载的药物释放到细胞质中杀死细胞。此间,Ga颗粒既起到能量转换增强的作用,又起到形状变换的作用。实验结果表明,包膜Ga颗粒在体肿瘤治疗具有极好的肿瘤治疗效果(图4,5)。

图4:Ga颗粒在体抗肿瘤冷冻治疗。(a)冷冻探针治疗荷瘤小鼠的热红外成像。(b)冷冻治疗过程中,冷冻探针表面的温度变化。(c)治疗过程中治疗组与对照组的荷瘤小鼠肿瘤体积变化。(d)治疗过程中荷瘤小鼠体重变化。(e)小鼠治疗过程中的存活率(左)和治愈率(右)曲线。(f)小鼠第1、7、14、21和77天的小动物活体成像,实时显示小鼠治疗过程中肿瘤体积变化。(g) 治疗结束后荷瘤小鼠的肿瘤组织H&E切片。
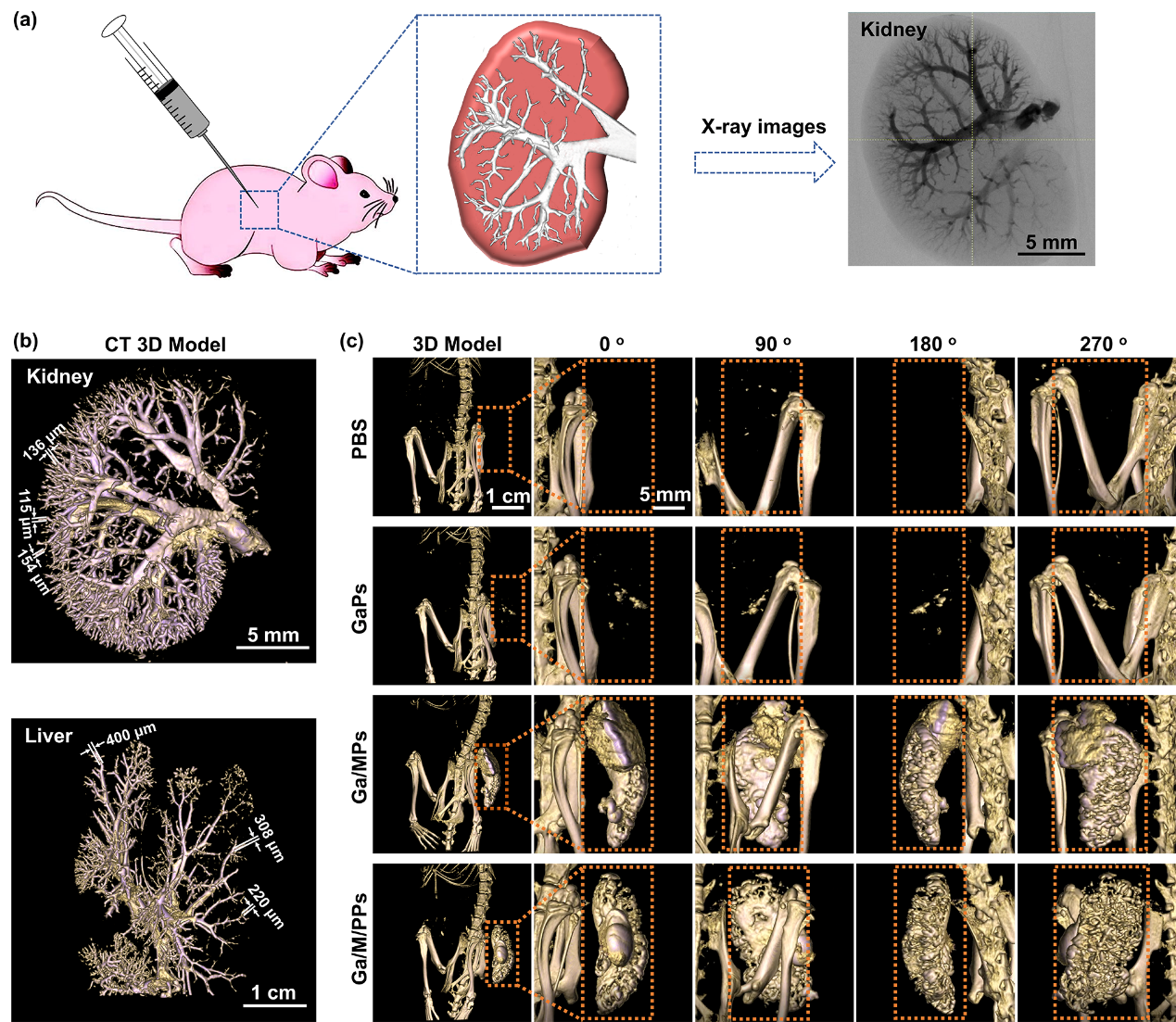
图5:Ga颗粒在离体器官和在体肿瘤的x射线高分辨率成像。(a) Ga颗粒在动物体内的注射及肾脏X成像示意。(b)大鼠肾脏、肝脏血管灌注Ga颗粒后的micro-CT三维成像。(c)在0o、90o、180o和270o条件下,三种Ga颗粒注射到肿瘤部位后的micro-CT成像。
此项研究首次实现了LM颗粒冷冻变形强化的细胞内治疗,在肿瘤临床治疗方面显示出潜在的应用前景。在未来研究中,该基于液态金属高效冷冻变形的细胞内肿瘤疗法有望作为一种通用的治疗策略,实现对如乳腺癌、肺癌、白血病等肿瘤的治疗,同时,由液态金属触发的肿瘤疗法有望与免疫治疗结合,实现物理机械破坏、物理消融、化疗与免疫治疗多模式的治疗机制,提高肿瘤治愈率。该工作得到国家自然科学基金重大项目、国家重点研发计划项目和中央高校基本科研经费等的大力支持。(来源:科学网)
相关论文信息:https://doi.org/10.1016/j.matt.2021.11.006