微生物所等发现抗结核活性新型abyssomicins化合物
结核病(tuberculosis,TB)是世界第二大致死性感染疾病,近年来由于结核感染与艾滋感染的协同作用、全球人员的不断流动、不合格的公共卫生项目、耐药性及感染的持久性等原因,使开发新型抗结核药物的需求更为迫切。中国科学院微生物所张立新实验室使用带有绿色荧光蛋白(GFP)表达载体的牛型结核分支杆菌Mycobacterium bovis减毒株bacillus Calmette-Guérin,即BCG 菌株作为测试菌株,建立了BCG高通量筛选模型作为抗TB活性成分的筛选,该方法高效直观且操作相对安全,为抗结核化合物的发现提供了快速通道。
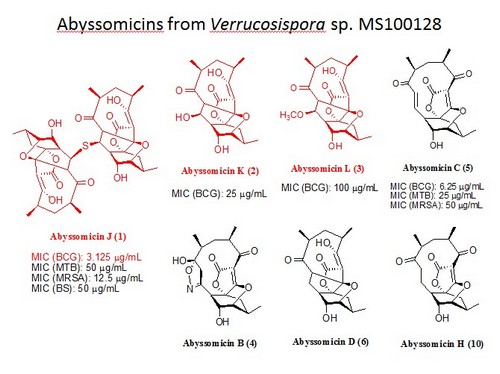
通过筛选课题组自主建立的微生物天然产物库,发现海洋疣孢菌Verrucosispora sp. MS100128的粗提物具有抗BCG活性。通过与澳大利亚昆士兰大学Robert Capon教授合作,获得了一系列结构新颖的微生物次级代谢产物abyssomicins,包括3个新化合物abyssomicin J、K、L和4个已知化合物abyssomicin B、C、D、H。其中abyssomicin J为首次发现的含硫原子二聚体结构的该类化合物,其显示出良好的抗BCG活性,MIC值为3.125 µg/mL。
在过去的研究表明,在这类化合物中,仅结构中含有α,β-不饱和酮活性基团的atrop-abyssomicin C与abyssomicin C才起生物学作用。张立新课题组发现,新颖结构含硫原子同源二聚体结构显示出更好的活性,论文通过化学半合成的方法发现了abyssomicin C可以通过迈克加成反应(Michael addition)转化为abyssomicin J、K、L,促进了对abyssomicin类化合物的化学反应性、稳定性和生物活性的深入理解。
同时,本研究进一步通过细胞水平的实验验证了abyssomicin J在BCG细胞内会自发转变为atrop-abyssomicin C而发挥其抗结核活性的初步假设,并揭示了该类化合物可以克服atrop-abyssomicin C不稳定的缺点,本论文的发现这为将此类化合物开发成成为新一代稳定的抗结核前体药物提供了理论依据。这些研究成果首次揭示了abyssomicin类化合物的硫醚迈克加成产物是更加稳定的且具有定高反应活性的Michael acceptor,具有更高的生物利用率和药效潜力,为研制新一类抗TB的临床药物奠定了基础。
相关论文:WANG Qian, SONG Fuhang, XIAO Xue, HUANG Pei, LI Li, Aaron Monte, Wael M. Abdel-Mageed, WANG Jian, GUO Hui, HE Wenni, XIE Feng, DAI Huanqin, LIU Miaomiao, CHEN Caixia, XU Hao, LIU Mei, Andrew M. Piggott, LIU Xueting*, Robert J. Capon*, ZHANG Lixin*. Abyssomicins from a South China Sea deep-sea sediment Verrucosispora sp.: Natural thioether Michael addition adducts as potential antitubercularprodrugs. Angewandte Chemie International Edition, 2012, DOI: 10.1002/anie.201208801 and 10.1002/ange.201208801(IF=13.455, 5-Year IF=13.195)(来源:中科院微生物研究所)
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。