中国科学院上海有机化学研究所研究员袁钧瑛院士、研究员周界文、副研究员刘建平团队,揭示了电偶极矩作用力驱动肿瘤坏死因子受体1(TNFR1)通路复合物I动态变化的结构基础,首次发现电偶极矩之间的长程相互作用在细胞信号转导中的重要生物学功能。4月1日,相关研究成果发表于《自然》。
TNFR1是一种多效能的跨膜受体,在细胞死亡、炎症和免疫中发挥关键作用。复合物I是一种包含众多组分的细胞内复合物,可以触发多种下游信号,这些信号的动态平衡决定了细胞是存活还是死亡。在体内,TNFR1结合配体TNFα引发的跨膜信号转导依赖于复合物I。
通过各自的死亡结构域,TNFR1与胞质内的肿瘤坏死因子受体相关死亡结构域蛋白(TRADD)和受体相互作用蛋白激酶1(RIPK1)结合,构成了复合物I的核心结构。该复合物具有高度动态变化的特点,但复合物I组装和解体的驱动机制一直是TNFR1领域内的未解之谜。
研究团队捕捉到了复合物I的核心,并用冷冻电镜技术解析了其高分辨率结构。这个核心包含来自TNFR1、TRADD和RIPK1的31个死亡结构域单元,组成一个包含6层五聚体的螺旋型纤维结构。在5个TRADD死亡结构域形成的五聚体上下表面,分别结合了两层TNFR1或RIPK1五聚体。
研究团队进一步发现,3种死亡结构域通过良好互补的静电表面形成特异性的相互作用,从而组装成高度有序的螺旋型复合物。3种死亡结构域形成的螺旋型纤维表面呈现出大量正负电荷高度分离的特征,导致3种死亡结构域寡聚体之间形成明显的远程电偶极矩相互作用。
值得一提的是,RIPK1寡聚体的电偶极矩方向与TNFR1和TRADD的方向相反,这也是RIPK1会被TNFR1/TRADD招募到细胞膜上的原因。此外,当RIPK1寡聚体累积的一定程度,相反的电偶极矩方向会产生排斥作用,抵消RIPK1与TRADD/TNFR1之间的吸引力,进而导致复合物I核心的解体,解释了TNFR1复合物I的动态行为。
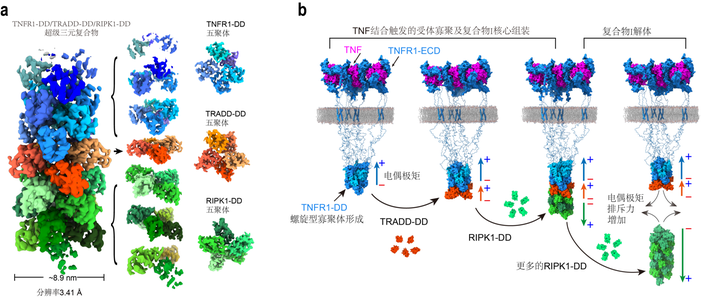 TNFR1信号复合物动态组装和解体的机制。研究团队供图
TNFR1信号复合物动态组装和解体的机制。研究团队供图
相关论文信息:http://doi.org/10.1038/s41586-026-10304-1
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。