中国科学技术大学傅尧教授、陆熹副教授、徐允河教授在碳-碳偶联合成手性有机硅烷方面取得进展。研究团队开发了丰产金属钴催化体系,成功实现硅基团导向的立体选择性碳-碳偶联反应,突破了传统不对称偶联对配位基团或共轭体系的依赖,为手性有机硅烷的精准合成提供了高效新方法。该研究成果于2025年8月22日以“Modular construction of α- or β-stereogenic organosilanes and organogermanes via enantioselective alkene hydroalkylation”为题发表在《自然·合成》(Nature Synthesis)。
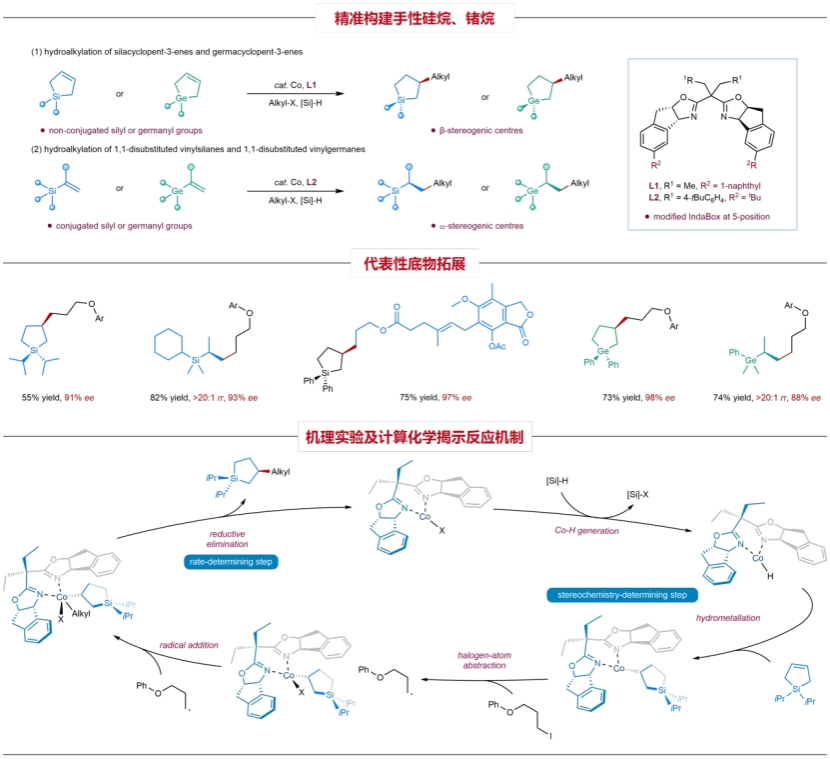
图1.碳-碳偶联合成手性有机硅烷、锗烷
有机硅烷在现代药物化学与复杂分子合成领域具有重要价值。作为碳的生物电子等排体,硅原子独特的原子半径与电负性差异可显著调控候选药物分子的亲脂性、膜渗透性等生理活性。在天然产物全合成领域,含硅手性模块已成为构建复杂分子的关键中间体。因此,发展手性有机硅烷的高效精准合成方法具有重要的科学意义。
烷基偶联反应通过碳链增长和碳骨架构建,成为创制复杂有机分子的重要策略。过渡金属催化烷基碳中心构筑通常依赖配位导向基团或π共轭体系实现区域与对映选择性控制。然而,硅基团缺乏共轭电子效应与定向配位能力,在不对称碳-碳偶联反应中难以作为有效的辅助基团发挥作用,导致该类反应极具挑战性。
研究团队开发了钴催化含硅、锗烯烃的不对称氢烷基化新策略。通过配体结构定向修饰,实现了对立体化学决定步骤——烯烃氢金属化步骤的选择性精准控制,建立了非共轭硅基团诱导的高区域选择性和高对映选择性控制新模式。该反应体系展现出宽广的底物适用范围和优异的官能团兼容性,对复杂药物分子修饰表现出良好的反应效果。所得β-手性硅化合物作为关键合成砌块,可经Tamao氧化反应高效转化为天然产物全合成的重要中间体——手性2-烷基-1,4-丁二醇。
研究团队与田长麟教授团队合作,开展了电子顺磁共振机理研究,揭示了烷基卤化物的自由基活化机制。系统的机理实验结合DFT计算表明:硅原子的引入通过电子效应有效调控了烯烃反应活性,降低了反应活化能垒;高立体选择性则主要源于配体与底物取代基间的空间位阻作用。
该项研究不仅为功能有机硅烷合成提供了新技术支撑,更为无配位和共轭基团底物的不对称偶联反应开发提供了重要范例。
论文第一作者为化学高层次人才培养中心博士生胡潇、安徽大学物质科学与信息技术研究院硕士生王陈、生命科学与医学部特任研究员于璐,通讯作者为傅尧教授和陆熹副教授。该项目得到国家自然科学基金、中国科学院战略性先导科技专项、中国科学院青年创新促进会、安徽省自然科学基金的资助和支持。
论文链接:https://www.nature.com/articles/s44160-025-00857-w
(化学与材料科学学院、精准智能化学全国重点实验室、科研部)
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。