|
|
|
|
|
严重 SARS-CoV-2 全基因组关联研究中新型嗅觉相关信号的基因水平分析揭示其与疾病死亡率相关 | MDPI COVID |
|
|
论文标题:Gene-Level Analyses of Novel Olfactory-Related Signal from Severe SARS-CoV-2 GWAS Reveal Association with Disease Mortality
论文链接:https://www.mdpi.com/2673-8112/5/12/206
期刊:COVID
期刊主页: https://www.mdpi.com/journal/covid
作者背景:本研究由来自哈佛大学陈曾熙公共卫生学院、麻省总医院/哈佛医学院和杜克大学医学院的研究人员合作完成。研究团队背景涵盖流行病学、生物统计学、肺与危重症医学及人群健康等多个方向,为本研究中临床结局与遗传学数据的整合分析提供了跨学科支持。
1. 研究背景
COVID-19 在美国曾连续三年位列主要死因前列,但患者之间的疾病严重程度差异很大。既往全基因组关联研究(genome-wide association study, GWAS)已经发现了一些与 COVID-19 严重程度相关的遗传位点,不过不少结果缺乏重复验证,也缺少明确的功能学解释,因此这些遗传信号离真正的临床应用还有距离。
在这一背景下,该研究聚焦于住院重症 COVID-19 患者的死亡结局,希望识别与 30 天和 60 天死亡风险相关的遗传变异,并结合基因水平分析、功能预测和表达数量性状位点分析(expression quantitative trait loci, eQTL),进一步评估相关位点的潜在生物学意义。
2. 研究内容
本研究共纳入 370 例重症 COVID-19 患者,均来自麻省总医院。研究对象包括重症监护病房患者,以及因低氧血症需氧疗支持的非重症监护病房住院患者。患者分别来自两轮疫情高峰期:2020 年 3 月至 6 月以及2021 年 1 月至 3 月。研究团队收集了患者的年龄、性别、种族/族裔、吸烟状态、体重指数、重症监护病房收治情况,以及 30 天和 60 天死亡等临床资料,并基于全血样本进行了低深度全基因组测序分型。
在遗传数据处理中,研究者首先对原始单核苷酸多态性位点(single nucleotide polymorphisms, SNPs)进行了严格质控。初始数据共包含 80,650,091 个 SNPs,经过性别一致性检查、缺失率筛选、去除 X 染色体位点、次要等位基因频率过滤及 Hardy–Weinberg 平衡检验后,最终保留 6,305,694 个 SNPs 进入后续分析。
随后,研究采用多变量 logistic 回归评估各 SNPs 与 30 天和 60 天死亡风险之间的关系,并校正年龄、性别、吸烟状态、重症监护病房状态、疫情波次以及前 10 个主成分等因素。除单个位点分析外,作者还进一步采用最优统一序列核关联检验(optimally adjusted sequence kernel association test, SKAT-O)开展基因水平分析,对 GWAS 中显著位点所在区域以及既往 COVID-19 宿主遗传学计划(COVID-19 Host Genetics Initiative, HGI)报道的候选基因区域进行验证。同时,研究结合基因型-组织表达数据库(Genotype-Tissue Expression, GTEx) 数据进行了 eQTL 分析,并利用 RegulomeDB、HaploReg、ENCODE 和 FAVOR 等工具对关键位点进行了功能预测。
表 1. 麻省总医院 370 例重症 COVID-19 患者的临床特征
|
Covariates
|
Number of Patients (%)
|
30 Day Deaths (%)
|
60 Day Deaths (%)
|
Median Survival Time (Days) a
|
|
Total
|
370
|
79 (21.4)
|
86 (23.2)
|
16.0
|
|
Age (Years)
|
|
|
|
|
|
<50
|
86 (23.2)
|
8 (10.1)
|
9 (10.5)
|
16.5
|
|
≥50
|
284 (76.8)
|
71 (89.9)
|
77 (89.5)
|
16.0
|
|
Race & Ethnicity
|
|
|
|
|
|
Non-Hispanic White
|
245 (66.2)
|
62 (78.5)
|
67 (77.9)
|
15.0
|
|
Hispanic
|
125 (33.8)
|
17 (21.5)
|
19 (22.1)
|
18.0
|
|
Sex
|
|
|
|
|
|
Male
|
231 (62.4)
|
58 (73.4)
|
63 (73.3)
|
16.0
|
|
Female
|
139 (37.6)
|
21 (26.6)
|
23 (26.7)
|
15.0
|
|
Smoking Status
|
|
|
|
|
|
Never
|
211 (57.0)
|
35 (44.3)
|
38 (44.2)
|
15.0
|
|
Former
|
127 (34.3)
|
31 (39.2)
|
35 (40.7)
|
17.0
|
|
Current
|
23 (6.2)
|
7 (8.9)
|
7 (8.1)
|
18.0
|
|
BMI (kg/m2)
|
|
|
|
|
|
≤25
|
84 (22.7)
|
19 (24.1)
|
23 (26.7)
|
16.5
|
|
>25
|
286 (77.3)
|
60 (75.9)
|
63 (73.3)
|
15.5
|
|
ICU Status
|
|
|
|
|
|
Floor
|
140 (37.8)
|
12 (15.2)
|
13 (15.1)
|
7.0
|
|
ICU
|
230 (62.2)
|
67 (84.8)
|
73 (84.9)
|
23.0
|
|
COVID Surge
|
|
|
|
|
|
Wave 1 b
|
203 (54.9)
|
40 (50.6)
|
41 (47.7)
|
19.0
|
|
Wave 2 c
|
167 (45.1)
|
39 (49.4)
|
45 (52.3)
|
13.0
|
BMI,体重指数;ICU,重症监护病房。Wave 1 指 2020 年 3–6 月入组患者,Wave 2 指 2021 年 1–3 月入组患者。中位生存时间按死亡或出院(以先发生者为准)计算。
3. 研究结果
研究结果显示,位于 RTP5 基因上的变异位点 rs7420371 G>A 是与死亡结局关联最显著的独立信号。在多变量分析中,携带 A 等位基因的患者,其 30 天死亡风险显著升高,OR = 2.32,95% CI 1.59–3.39;其 60 天死亡风险同样升高,OR = 2.06,95% CI 1.43–2.97。这提示该位点与住院重症 COVID-19 患者的不良结局存在显著关联。
在基因水平分析中,作者进一步发现,RTP5 区域的 SNP 集合与 30 天和 60 天死亡风险均显著相关,p 值分别为 5.90 × 10-5 和 6.17 × 10-5。除 RTP5 外,既往 HGI 报道的多个候选基因区域也显示出与死亡结局的统计学关联,包括 SFTPD、MUC5B、ELF5、FBRSL1、SLC22A31、TMPRSS2、NR1H2 和 THBS3。这表明,部分与 COVID-19 住院或重症相关的遗传信号,也可能参与了住院后死亡风险的形成。
表 2. 主要遗传信号与重症 COVID-19 患者 30 天和 60 天死亡风险的关联
|
MGH COVID Genotypes (n = 370)
|
|
Mortality
|
SNPs a
|
Chromosome
|
Allele
|
MAF
|
Gene
|
FDR b
|
Bonferroni c
|
OR (95% CI) d
|
SE
|
|
30-day
|
rs7420371
|
2
|
G>A
|
0.3926
|
RTP5
|
0.017
|
0.031
|
2.32 (1.59, 3.39)
|
0.19
|
|
60-day
|
rs7420371
|
2
|
G>A
|
0.3926
|
RTP5
|
0.027
|
0.050
|
2.06 (1.43, 2.97)
|
0.19
|
SNP,单核苷酸多态性位点;MAF,次要等位基因频率;FDR,错误发现率;OR,比值比;SE,标准误。分析结果已校正年龄、性别、吸烟状态、疫情波次和主成分等因素。
表 3. RTP5 及 HGI 候选基因区域的 SKAT-O 分析结果
|
Mortality Outcomes p-Value
|
|
Top GWAS Signal & HGI Signals
|
30-Day Mortality b,c
|
60-Day Mortality b,c
|
|
RTP5 d
|
5.90 × 10−5
|
6.17 × 10−5
|
|
SFTPD
|
2.04 × 10−5
|
3.85 × 10−5
|
|
MUC5B
|
1.42 × 10−5
|
3.46 × 10−5
|
|
ELF5
|
2.41 × 10−6
|
1.10 × 10−5
|
|
FBRSL1
|
1.76 × 10−5
|
2.23 × 10−5
|
|
SLC22A31
|
1.69 × 10−5
|
1.55 × 10−5
|
|
TMPRSS2
|
2.17 × 10−5
|
3.31 × 10−5
|
|
NR1H2
|
0.0001
|
0.0002
|
|
THBS3
|
0.0013
|
0.0006
|
进一步的 eQTL 分析显示,rs7420371 的 A 等位基因与脑组织中 RTP5 表达升高显著相关。其中,在小脑(266 个样本)中,p = 1.77 × 10-6;在小脑半球(277 个样本)中,p = 4.39 × 10-3;在大脑皮层(270 个样本)中,p = 1.83 × 10-2。相比之下,在肺组织和全血中,该位点与 RTP5 表达未见显著相关。功能预测结果也提示,该位点可能具有一定调控活性及潜在生物学意义。
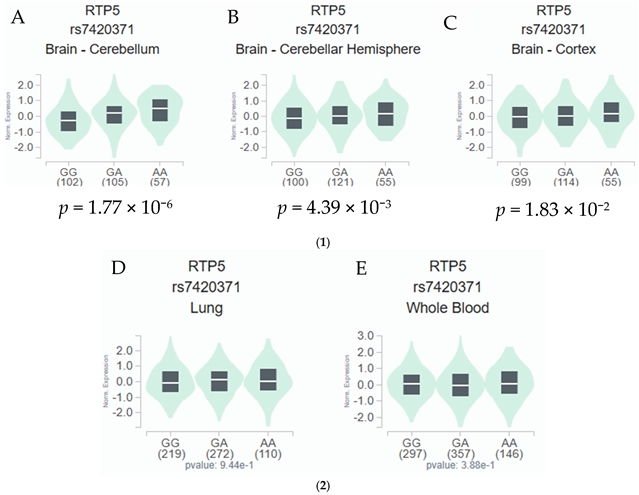
图 1. rs7420371 G>A 与 RTP5 在不同组织中的 eQTL 分析结果。A 等位基因与小脑、小脑半球和大脑皮层中 RTP5 表达升高显著相关,而在肺组织和全血中未见显著关联。eQTL,表达数量性状位点。
4. 结论与展望
总体来看,该研究在住院重症 COVID-19 患者中识别出一个新的、可能具有功能意义的遗传位点 RTP5 rs7420371 G>A,并通过基因水平分析和 eQTL 结果为其潜在作用提供了支持。研究提示,RTP5 相关变异可能不仅与 COVID-19 中的嗅觉和味觉异常有关,也可能参与疾病重症结局的形成。这项研究为 COVID-19 死亡风险相关遗传机制提供了新的线索,也为后续围绕 RTP5 的功能研究提供了基础。
原文出自 COVID 期刊
Zhao, Y.C.; Wang, X.; Lu, Y.; et al. Gene-Level Analyses of Novel Olfactory-Related Signal from Severe SARS-CoV-2 GWAS Reveal Association with Disease Mortality. COVID 2025, 5, 206.
COVID(ISSN 2673-8112)是由MDPI出版社每月在线出版的国际性、经过同行评审的开放获取期刊,致力于冠状病毒及其相关疾病与全球影响的多学科研究。本刊旨在为冠状病毒研究的各个领域提供高端学术交流平台,涵盖基础分子与临床研究、公共卫生、心理健康、经济与环境影响等广泛主题。
期刊收录范围包括但不限于:
• 人类与动物冠状病毒:流行病学与进化、病毒跨物种传播、病毒-宿主相互作用等
• 临床治疗:病毒性呼吸道感染、冠状病毒肺炎、免疫反应等
• 治疗研发:疫苗设计、抗病毒药物、单克隆抗体、诊断技术等
• 公共卫生:疫情防控、流行病学模型、社会隔离影响、疫苗接种等
• 全球影响:经济影响、生活方式变化、环境效应、供应链管理等

特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。