|
|
|
|
|
肠黏液中的磷脂酰胆碱可抵御微生物群的黏膜侵袭及继发炎症| MDPI Livers |
|
|
论文标题:Phosphatidylcholine in Intestinal Mucus Protects against Mucosal Invasion of Microbiota and Consequent Inflammation
论文链接: https://www.mdpi.com/2673-4389/4/3/34
期刊名:Livers
期刊主页: https://www.mdpi.com/journal/livers
文章导读
该综述以肠道黏液中磷脂酰胆碱(PC)的黏膜保护作用为核心,系统阐述了其作为肠道黏液疏水屏障关键成分的机制:PC通过肠道上皮紧密连接(TJ)旁细胞转运至黏液层,先与膜结合型黏蛋白MUC3结合,再转移至分泌型黏蛋白MUC2,形成阻挡菌群侵袭的物理屏障。文章明确指出,溃疡性结肠炎(UC)患者存在固有且特征性的黏液PC缺乏,其根源在于紧密连接受损导致PC转运受阻;携带外磷脂酶的肠道菌群过度增殖会进一步降解黏液PC,使其含量降至30%临界水平以下,触发急性黏膜炎症。文章以幽门螺杆菌为例,印证了外磷脂酶阳性菌的致病作用。 在此基础上,综述梳理了两种靶向治疗策略:一是肠腔局部补充迟释型PC制剂,填补黏蛋白PC结合空位并为外磷脂酶阳性菌群提供替代营养源,多项2期临床试验已证实其疗效;二是应用非吸收性磷脂酶抑制剂(如UDCA-LPE),通过结合宿主细胞内iPLA2β抑制炎症介质LPC生成,动物实验显示其可降低粪便PLA2活性、改善炎症指标并恢复菌群正常分布。文章还将该机制拓展至肝胆疾病,提出利用胆肝循环通过肝细胞ABCB4转运体补充胆道PC以治疗原发性硬化性胆管炎(PSC)的思路。最后,文章指出鉴定外磷脂酶阳性菌种类、优化PC制剂及验证临床效果等是未来核心研究方向,为肠道及肝胆炎症性疾病的研究与治疗提供了重要依据。
肠道黏液磷脂酰胆碱屏障的形成机制及溃疡性结肠炎的转运缺陷
磷脂酰胆碱(PC)是肠道黏液疏水屏障的核心关键成分。血液中的PC以无脂蛋白组分形式,经肠道上皮紧密连接旁细胞转运至黏液层,在顶端负电位驱动下,通过带正电的胆碱头部与膜结合型黏蛋白MUC3结合,再转移至分泌型黏蛋白MUC2,形成可有效阻挡菌群侵袭的疏水屏障(黏液中超过90%的磷脂为PC和溶血磷脂酰胆碱),且该屏障的形成不影响肠道正常的水盐与营养吸收。文章进一步明确,溃疡性结肠炎(UC)存在固有且特征性的黏液PC缺乏:即使患者处于临床缓解期,黏液PC含量也显著降低约70%,导致黏液疏水性显著下降、疏水屏障功能受损。这一缺陷的核心根源在于UC患者肠道上皮紧密连接受损,造成PC的旁细胞转运受阻,无法正常富集于黏液层。
菌群的 PC 降解作用与幽门螺杆菌典型例证
道菌群是造成溃疡性结肠炎患者黏液磷脂酰胆碱(PC)进一步损耗并触发急性黏膜炎症的关键因素。部分肠道共生菌可表达外磷脂酶,这类外磷脂酶阳性菌能将黏液中的PC作为营养源进行降解。当该类菌群过度增殖时,会进一步消耗UC患者本就匮乏的黏液PC,使其含量降至30%的保护临界水平以下,从而破坏黏液疏水屏障,导致菌群侵袭黏膜,引发急性炎症。同时,UC的炎症微环境又会进一步促进外磷脂酶阳性菌群富集,形成恶性循环。幽门螺杆菌是典型的PC降解型外磷脂酶阳性菌:它通过表达磷脂酶A2降解胃黏膜中的PC,破坏胃黏膜疏水屏障;同时还能损伤胃上皮紧密连接,进一步减少PC分泌,最终引发胃窦炎甚至溃疡。未成熟香蕉富含PC,既可填补胃黏膜黏蛋白的PC结合位点,又能为幽门螺杆菌提供替代营养源,从而减少其对黏膜自身PC的降解。这一现象也印证了外磷脂酶阳性菌通过消耗PC介导黏膜损伤的致病作用。
PC局部替代治疗UC的研发应用及其他肠病的潜在价值
基于肠道黏液PC缺乏的病理机制,临床研发了结肠/回结肠靶向释放的PC制剂用于局部替代治疗溃疡性结肠炎(UC)。该制剂通过肠溶包衣避免被胰腺酶降解,实现PC的靶向补充;多项2期临床试验及荟萃分析证实,1.5-3.0 g/天的PC治疗能剂量依赖性诱导UC缓解、显著减轻黏膜炎症,对激素难治性UC也具备疗效,可减少激素用量并改善患者生活质量,且在2期试验中未观察到严重不良反应。然而,3期试验因强制联用美沙拉嗪(后者具有洗涤剂样作用,阻碍PC与黏蛋白结合)而未能达到预期终点。其核心作用机制为双重保护:一方面填补UC患者黏蛋白的PC结合空位、重建黏液疏水屏障;另一方面为外磷脂酶阳性菌群提供替代营养源,减少其对宿主黏液PC的降解。
对于克罗恩病等同样存在肠道上皮紧密连接缺陷、可能伴随黏液PC缺乏的炎症性肠病,PC局部替代治疗的潜在效果基于紧密连接-PC转运机制的合理推测,尚未得到实验与临床的直接证实,相关疗效仍需进一步研究验证。
总结与展望
该综述得出结论,黏液磷脂酰胆碱(PC)缺乏是肠道黏膜炎症发生发展的关键病理环节,携带外磷脂酶的肠道菌群过度增殖降解黏液PC,是打破UC患者黏膜保护临界水平、触发急性炎症的核心因素。肠腔局部补充PC可通过重建疏水屏障、为外磷脂酶阳性菌群提供替代营养源发挥保护作用;而非吸收性磷脂酶抑制剂则通过结合宿主细胞内钙非依赖性膜磷脂酶A2β(iPLA2β),抑制炎症介质溶血磷脂酰胆碱(LPC)的生成,动物实验显示其可降低粪便PLA2活性、改善炎症指标并恢复肠道菌群正常分布,二者均为靶向该病理环节的有效治疗策略。研究同时展望,未来需进一步鉴定肠道中具体的外磷脂酶阳性菌种类并明确其磷脂酶活性与肠道炎症的关联,优化PC制剂的给药方案并规避美沙拉嗪等去垢剂类药物的联用干扰,验证磷脂酶抑制剂的临床疗效及菌群移植在调节肠道菌群组成中的作用;此外,还需深入探究肝肠PC代谢的调控机制,推动PC相关治疗策略在原发性硬化性胆管炎等肝胆疾病中的转化应用,为肠道及肝胆系统炎症性疾病的病理机制研究和临床治疗开发提供更坚实的理论与实践支撑。
图 1. 磷脂酰胆碱 (PC)
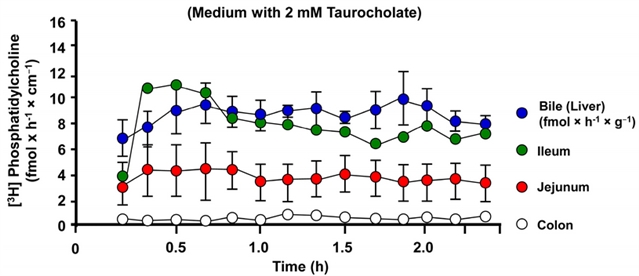
图 2. 磷脂酰胆碱 (PC) 分泌到体内灌注的大鼠肠段。
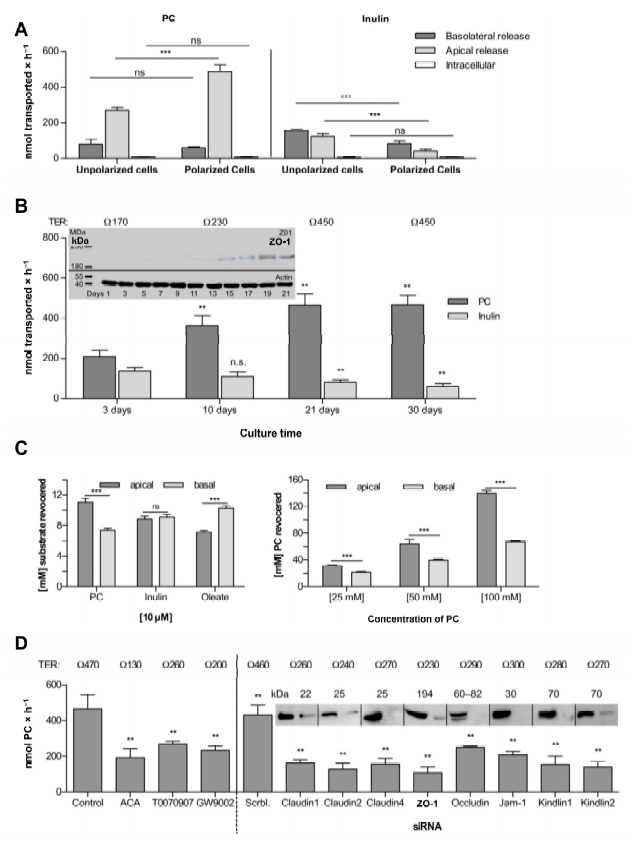
图 3. 在 CaCo2 细胞的 Transwell 组织培养系统中检测磷脂酰胆碱通过紧密连接的转运
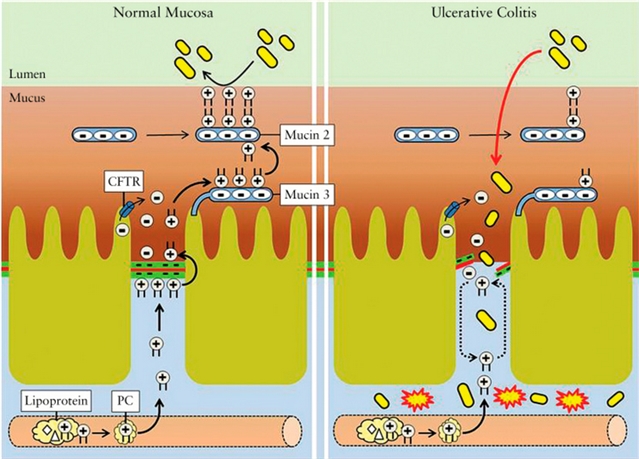
图 4. 正常黏膜中保护性磷脂酰胆碱粘液层的形成示意图以及溃疡性结肠炎中由于紧密连接紊乱导致磷脂酰胆碱粘液层紊乱的病理生理学
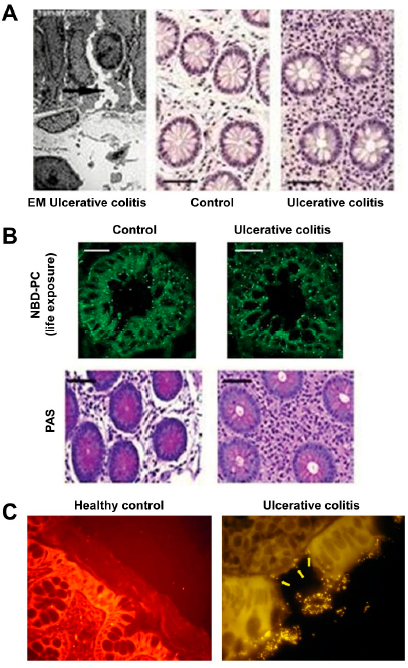
图 5. 人类溃疡性结肠炎(缓解期)中由于紧密连接紊乱导致隐窝扩大,从而损害管腔 PC 的积累,并导致细菌侵入有缺陷的粘液层
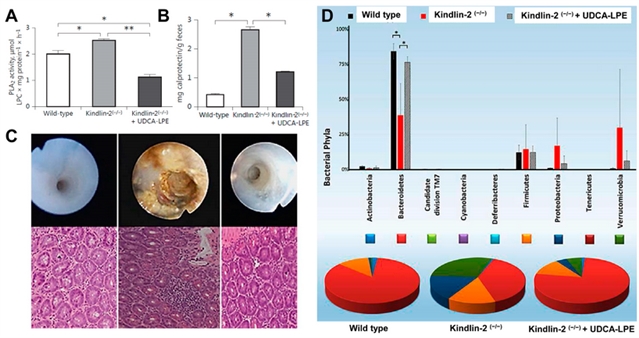
图 6. 野生型小鼠与溃疡性结肠炎小鼠(用他莫昔芬诱导的 kindlin-2−/− 小鼠)和用磷脂酶抑制剂熊去氧胆酸-溶血磷脂酰乙醇胺 (UDCA-LPE) 治疗的溃疡性结肠炎小鼠的比较。
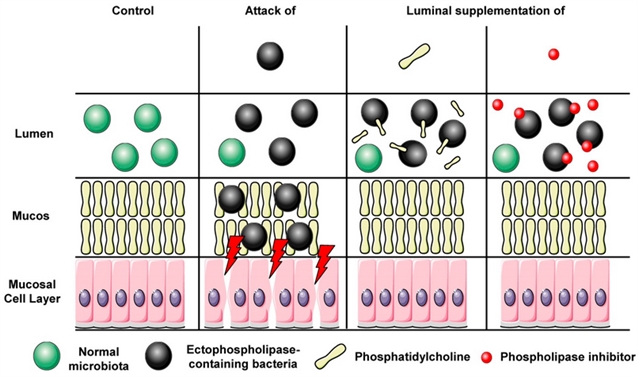
图7. 含外磷脂酶的细菌攻击黏液磷脂酰胆碱的示意图
Livers期刊主题涵盖肝炎 所有形式;酒精性肝病;非酒精性脂肪性肝病和非酒精性脂性肝炎;肝硬化;胆道疾病;药物性肝损伤;遗传性和代谢性肝病及其并发症;癌症与药物代谢;肝细胞癌;肝纤维化;肝病免疫学;肝病学营养;肝病病理学;肝病的诊断和治疗,为肝病学多学科领域的基础、转化和高级临床研究提供平台。目前已被 ESCI(Web of Science)、Scopus 等国际权威数据库收录。
|
|
主编: Prof. Dr. Hartmut W. Jaeschke
University of Kansas Medical Center, Kansas City, KS 66160, USA
|
|
|
副主编:Prof. Dr. Ralf Weiskirchen
RWTH University Hospital Aachen, D-52074 Aachen, Germany
|
|
2024 Impact Factor
|
2.4
|
|
2024 CiteScore
|
3.2
|
|
Time to First Decision
|
27
|
|
Time to Publication
|
6.7
|
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。