|
|
|
|
|
磁性微针阵列机器人实现可控组织切割 助力高通量药物筛选 Engineering |
|
|
论文标题:Controllable Histotomy Based on Hierarchical Magnetic Microneedle Array Robots
期刊:Engineering
DOI:https://doi.org/10.1016/j.eng.2024.05.004
微信链接:点击此处阅读微信文章

东南大学、南京鼓楼医院及中国科学院大学温州研究院的研究团队在《Engineering》期刊发表一项新型生物医学技术研究成果。该团队开发出基于分级磁性微针阵列机器人的可控组织切割技术,为原代组织的精准加工与高通量药物筛选提供了新方案,在临床精准医疗领域展现出应用潜力。
患者来源的原代组织体外培养在精准诊断、个性化用药、个体化治疗及组织工程等领域具有重要价值。其中,患者来源的原代肿瘤组织培养因保留了与患者组织相似的生物学特征,且对培养条件要求相对宽松,被认为是反映患者实际病情最便捷、最具指导性且最可靠的方法之一。为实现肿瘤治疗与预后评估,从原代肿瘤组织构建 “肿瘤芯片” 开展高通量药物筛选,已成为研究热点。当前,原代组织的提取与培养通常需获取临床组织样本后,手工切割成小于立方毫米级的不规则小块,再置于培养基中体外培养。但手工切割存在精度不足、依赖操作经验、组织块形态随机不规则难以标准化,以及后续分离与操控困难等问题,开发新型临床组织切割与培养策略十分必要。
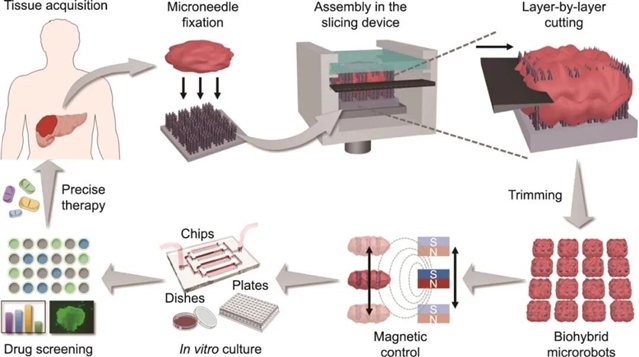
图1 肿瘤组织切割、操控与培养用于高通量药物筛选的示意图。原代组织通过磁性微针支架固定,并借助切割装置切割成小块组织;由于封装有微针碎片,这些组织块获得了磁响应特性。随后,这些组织块可被培养于孔板、培养皿或微流控芯片中,从而实现药物筛选并指导精准治疗。
针对这些问题,研究团队提出了可控组织切割技术,其核心是3D打印的榫卯结构切割装置与加载磁性颗粒的宝塔状微针阵列支架。该微针支架由磁性微针阵列和非磁性基材组成,制备过程中先通过3D打印机打印有序微针阵列的3D模具,经Ecoflex硅橡胶脱模获得阴模,再向阴模中注入含钕铁硼(NdFeB)磁性粒子的预聚物,经紫外辐射固化后完成制备。所制微针共由六个层级构成,总长度约为1400 μm,每一层的高度与底部直径分别集中在230 μm与188 μm左右,足以完全穿透组织样本。
在组织切割过程中,微针支架被压在组织上,通过机械嵌合方式将组织固定在微针尖端,有效防止切割时组织滑移。实验数据显示,多层结构微针支架的最大拔出力是光滑表面微针支架的4.66倍,机械嵌合效应还延长了微针支架与组织的连接时间。固定后的组织与微针支架一同安装在承载架上并插入外壳内,盖板安装在最上层的槽中,支架通过承载架抬起与盖板接触,外科手术刀片从底部槽滑入进行切割。由于相邻槽的间距设置为0.5 mm,每次上移都会切割出薄薄的组织切片,经外部磁铁收集切片并重复切割循环,最后用手术刀修整,可获得尺寸小于1.0 mm × 1.0 mm × 0.5 mm(长 ×宽 × 厚)的均一组织块,满足原代组织体外培养的临床标准。
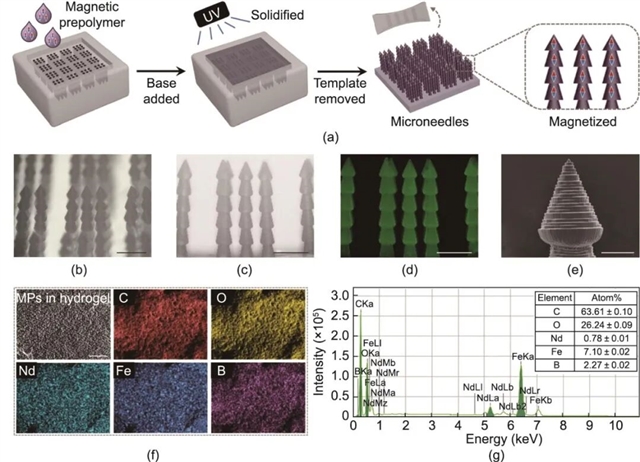
图2 微针支架的制备与表征。
值得关注的是,微针碎片中包封的磁性材料使切割后的组织片段具备磁响应性,可转化为生物混合微型机器人。这些组织块在磁化后获得固定磁极性,在外加磁场作用下能实现定向移动、旋转运动等可控操作,多个生物混合微型机器人还可在同一旋转磁场中同步驱动并沿独立路径运动。细胞相容性评估显示,肿瘤细胞与磁性微针支架共培养时,仍表现出良好的黏附与增殖能力,为后续原代组织培养奠定了基础。
研究团队进一步构建了多层微流控芯片系统,该芯片通过逐层模板复制和封装过程制备,包含四个输入口、六十个反应室(按四个一组分组)和十五个输出口,可进行十五种不同的实验药物组合。生物混合微型机器人借助磁铁与刮板可被便捷地填充入微流控芯片的各个反应室,刮板能清除错位组织块并确保每个反应室仅含一个组织块,芯片下方的磁铁则将组织块吸附于反应室底部,保障培养过程的稳定性。
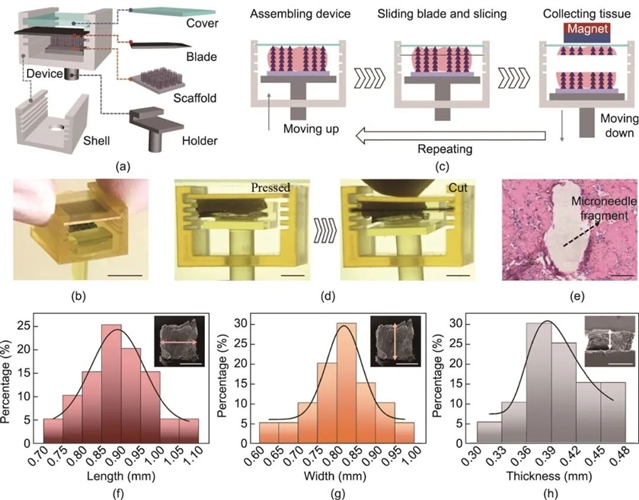
图3 通过组织切割装置处理的肿瘤组织。(a)组织切割装置各组件结构的示意图;(b)组织切割装置的光学图像;(c)组织切割过程的操作示意图;(d)切割小鼠肿瘤组织的现场图像;(e)含微针碎片的组织块H&E染色图像;从五份肿瘤样本中收集的20块组织的长度(f)、宽度(g)和厚度(h)分布。比例尺:(c)为5 mm,(d)为2 mm,(e)为100 µm,(f)~(h)插图为500 µm。
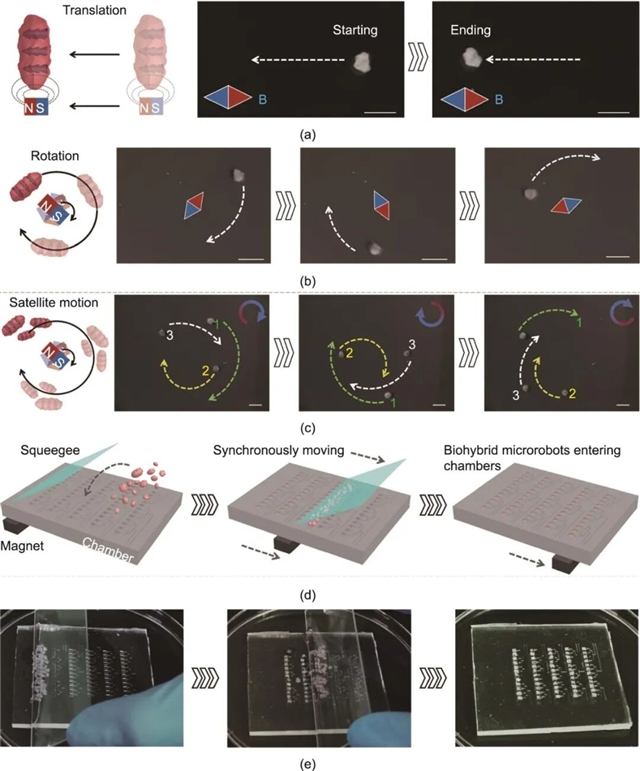
图4 生物混合微型机器人的磁控操纵。(a)单个生物混合微型机器人在恒定磁场下进行平移运动;(b)单个生物混合微型机器人在旋转磁场下进行旋转运动;(c)多个生物混合微型机器人在旋转磁场下同步旋转运动;(d)利用刮板与磁铁将生物混合微型机器人填充入微流控芯片反应室的示意图;(e)填充过程的实物图像。比例尺:(a)~(c)为2 mm。
为验证技术效果,研究团队以小鼠来源胰腺癌组织为样本,利用四种临床常用抗肿瘤药物(5-氟尿嘧啶、奥沙利铂、吉西他滨和紫杉醇)开展高通量药物筛选实验。药物工作溶液通过蠕动泵以1 mL/h的速度注入微流控芯片,形成单药、双药、三药及四药联合等十五种组合。培养三天后,通过钙黄绿素-AM(活细胞标记)和碘化丙啶(PI,死细胞标记)染色,结合 ImageJ 软件分析荧光图像,计算各组活细胞与死细胞比值。结果显示,对照组活细胞与死细胞比值为 9.77 ± 2.19,所有药物处理组的比值均显著下降至 1.5 以下,其中四药联合组活细胞与死细胞比值最低,仅为 0.78 ± 0.13,证实多药联合治疗的抗肿瘤效果优于单药治疗,与已有临床研究结论高度一致。
此外,免疫组织化学染色结果显示,胰腺癌标志物 MUC1、细胞生长因子受体 EGFR 以及增殖标志物 Ki67 均在芯片培养的组织块中大量表达,表明组织块在培养期间仍保持其功能性与高度活性。扫描电子显微镜观察与 H&E 染色结果也显示,肿瘤组织中的癌细胞保留了典型的恶性特征,说明该技术未破坏组织的生物学属性。
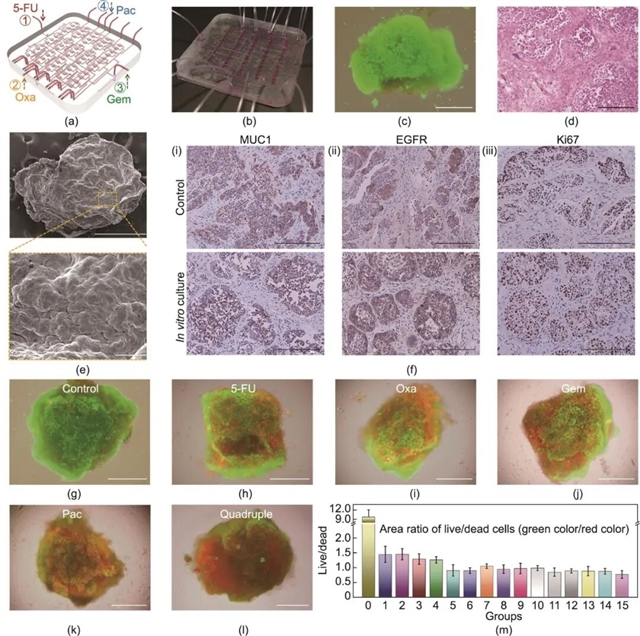
图5 微流控辅助抗癌药物筛选。(a)微流控芯片结构示意图,四种输入药物分别为5-FU、Oxa、Gem与Pac;(b)带有胰腺癌组织块的微流控芯片实物图;(c)培养3天后的胰腺癌组织块明场/荧光融合图像;(d)培养组织块的H&E染色图像;(e)培养组织块的SEM图像;(f)新鲜小鼠肿瘤组织与体外培养组织的免疫组织化学染色图像,包括MUC1(i)、EGFR(ii)与Ki67(iii);无药处理(g)、单药处理[(h)~(k)]以及联合用药(l)下的组织块明场/荧光融合图像,分别为5-FU(h)、Oxa(i)、Gem(j)、Pac(k)、四药联用(l);(m)各组组织块中活细胞与死细胞面积比值统计。组别说明:组0为对照组(未处理),组1~15依次对应不同单药及多药组合。比例尺:(c)、(e)上半部分和(g)~(l)为500 µm,(d)、(f)为200 µm,(e)下半部分为50 µm。
研究团队表示,未来将进一步提升该技术的自动化水平,在切片厚度控制与组织块三维定位方面进行优化,例如通过网格状刀架实现组织块横向切割,利用芯片底部布设的微型电磁线圈阵列配合机械臂与程序控制,实现组织块的自动化精确定位与排错。同时,还将拓展技术应用范围,适用于新型靶向药物与基因疗法筛选,以及皮肤、睾丸、肝脏、肾脏等其他原代组织的长期培养与动态观察,为生物医学研究与临床应用提供更广泛的技术支持。
论文信息:
Xiaoxuan Zhang,Hanxu Chen,Taiyu Song,Jinglin Wang,Yuanjin Zhao. Controllable Histotomy Based on Hierarchical Magnetic Microneedle Array Robots. Engineering, 2024, 42(11): 175-183 DOI:10.1016/j.eng.2024.05.004
更多内容
东南大学团队:仿生类红细胞微球助力组织工程
中国海洋大学团队:双层多糖水凝胶助力益生菌肠道靶向口服给药
《工程(英文)》:引领工程科技创新 服务国家战略需求
喜报:Engineering海外传播斩获佳绩!
Engineering征稿启事:人工智能赋能工程科技
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。