|
|
|
|
|
科学家把蛋白质设计成“磁性拼块”,向系统化材料迈进 |
|
|
2025年7月31日,美国华盛顿大学蛋白质设计研究所(IPD)David Baker与王顺智团队在Nature Materials期刊发表题为“Bond-centric modular design of protein assemblies”的新成果,他们借鉴“化学键”理念,把蛋白质零件做成会自动对准方向的“磁性拼块”。同一套零件可反复拆搭、按需变形、轻松定制,为结构材料、活体传感和分子机器奠定基础。一次性打包生成20余种封闭笼体、二维薄片、三维晶格和动态重构网络,设计实验成功率最高可达50%。
受限于天然蛋白界面复杂性,尽管蛋白质从头设计已取得长足进展,现有策略仍难以在原子级精度下自由拼搭大尺度、多组分且可重构的纳米结构。原因在于:
1.方向不可控——零件若角度稍有偏差便无法正确配对或导致无序聚集;2.接口不通用——每换一种目标结构就需重新设计全部接点,费时耗力、难以量产。
化学键的“价数+方向性+键能”思想能产生丰富结构,但如何迁移至蛋白质组装仍是难题。为此,团队提出“以键为核心”(bond-centric)模块化概念:

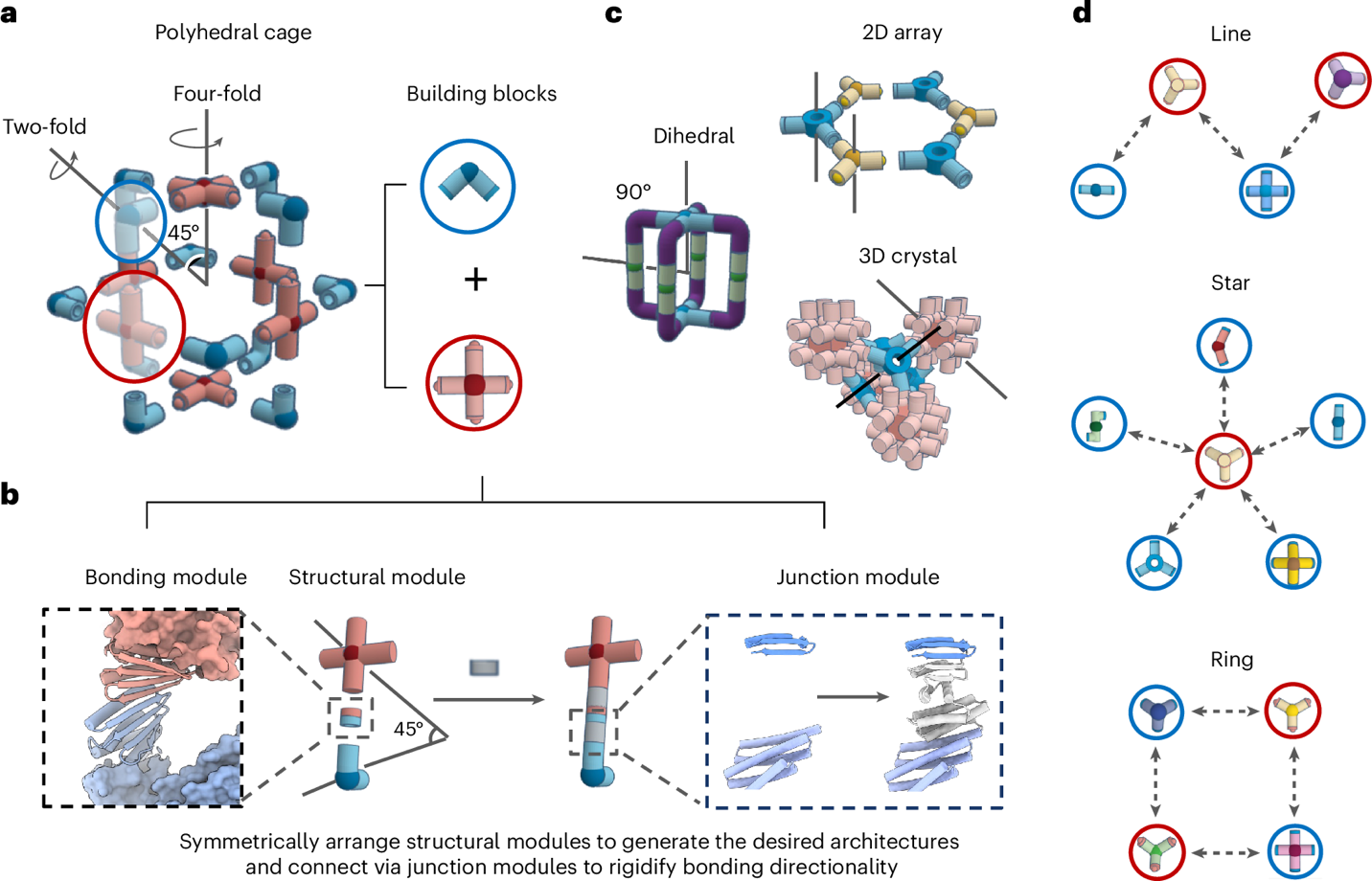
图1:以键为核心”(bond-centric)模块化设计流程示意 (图1)。
借助深度学习生成模型(如RFdiffusion)与传统工具(WORMS)精准控制作用朝向形成“链接模块”。研究者把“谁连谁、角度多少度”写进拼装脚本,AI 即可生成自动“对号入座”的零件,实现乐高式自由拼搭。
主要成果
1.多层级架构库 (图2)
成功设计并验证20余种多组分多面体蛋白笼、二维阵列与三维晶格,实验成功率达10–50?%,电镜结构与模型高度吻合。
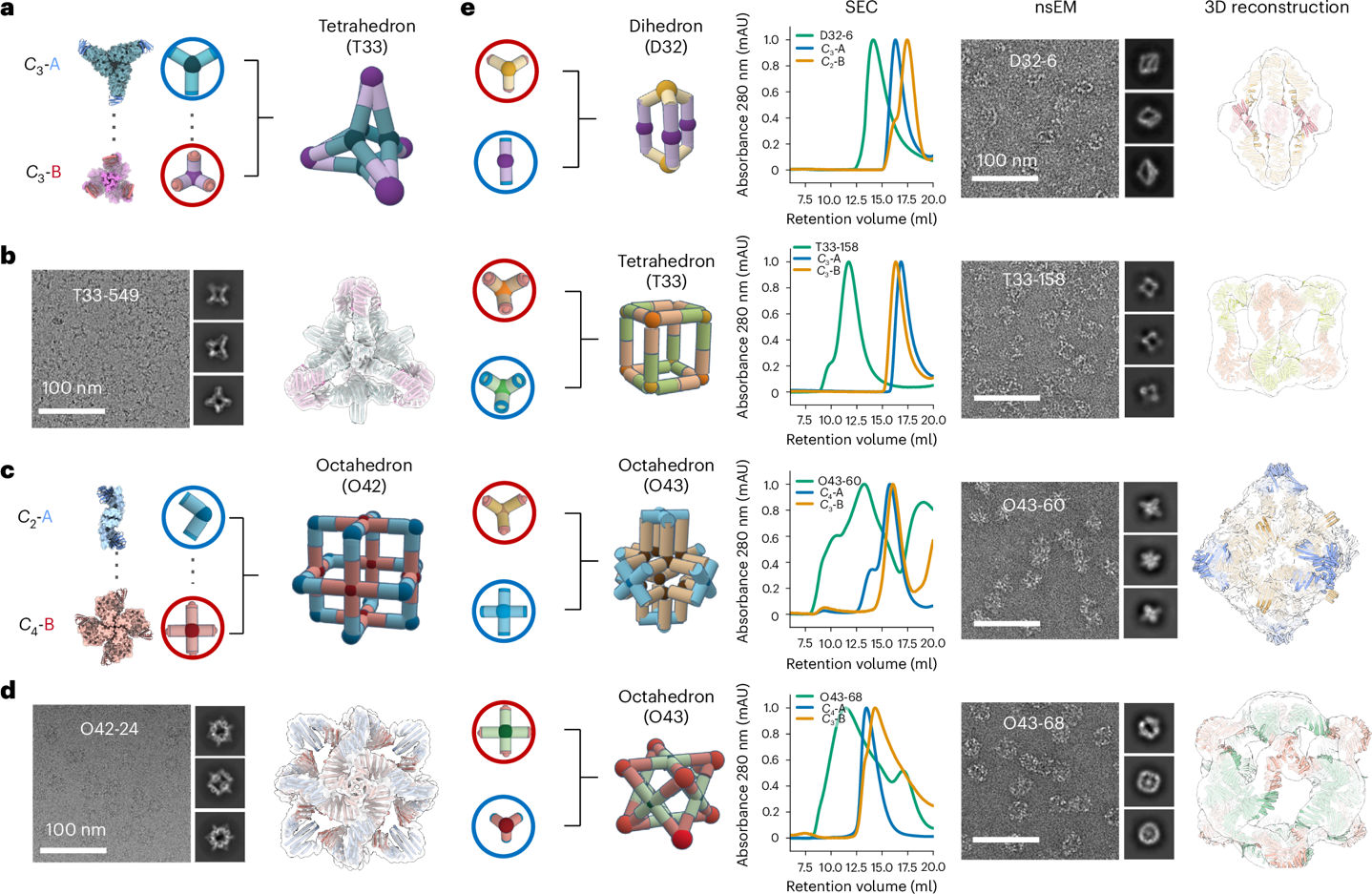
图2
2.零件复用与网络化组装(图3)
共享同一键模块的构筑单元可与不同伙伴快速重组合,构建星形、线形、环形等拓扑网络,大幅提升“经济造件”能力。
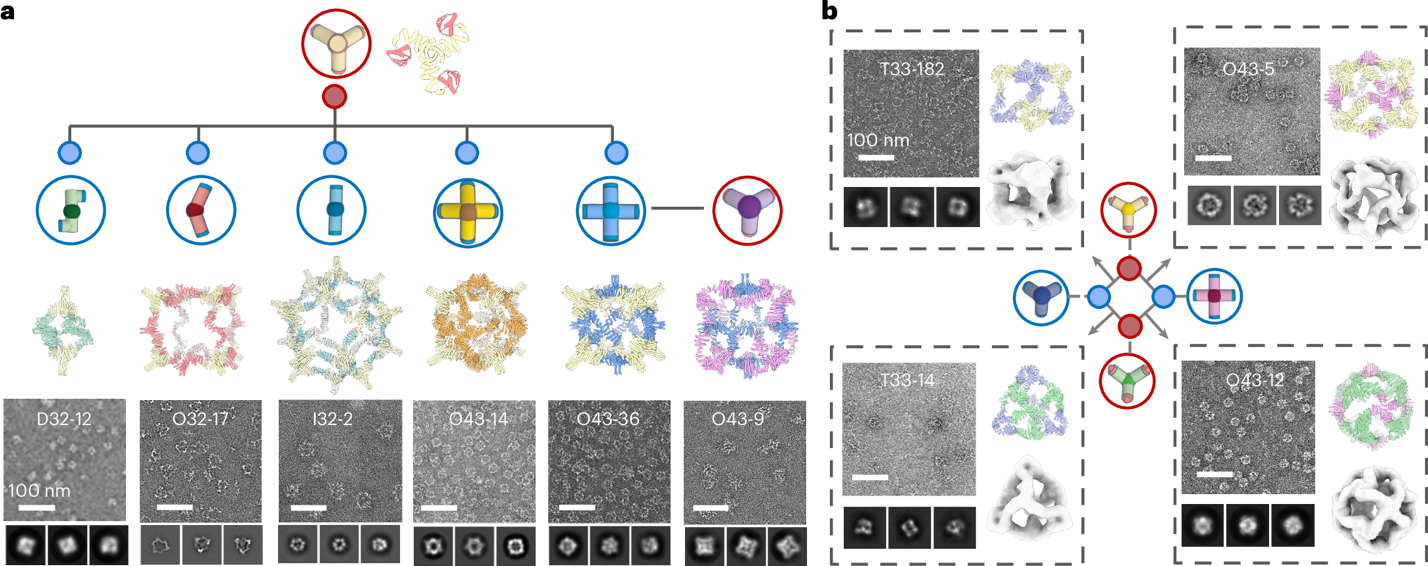
图3
3.动态可逆重构(图4)
基于共享构件,可实现笼体↔二维层的可控转换,揭示不同形态之间的能量与动力学偏好,为可编程纳米机械奠基。
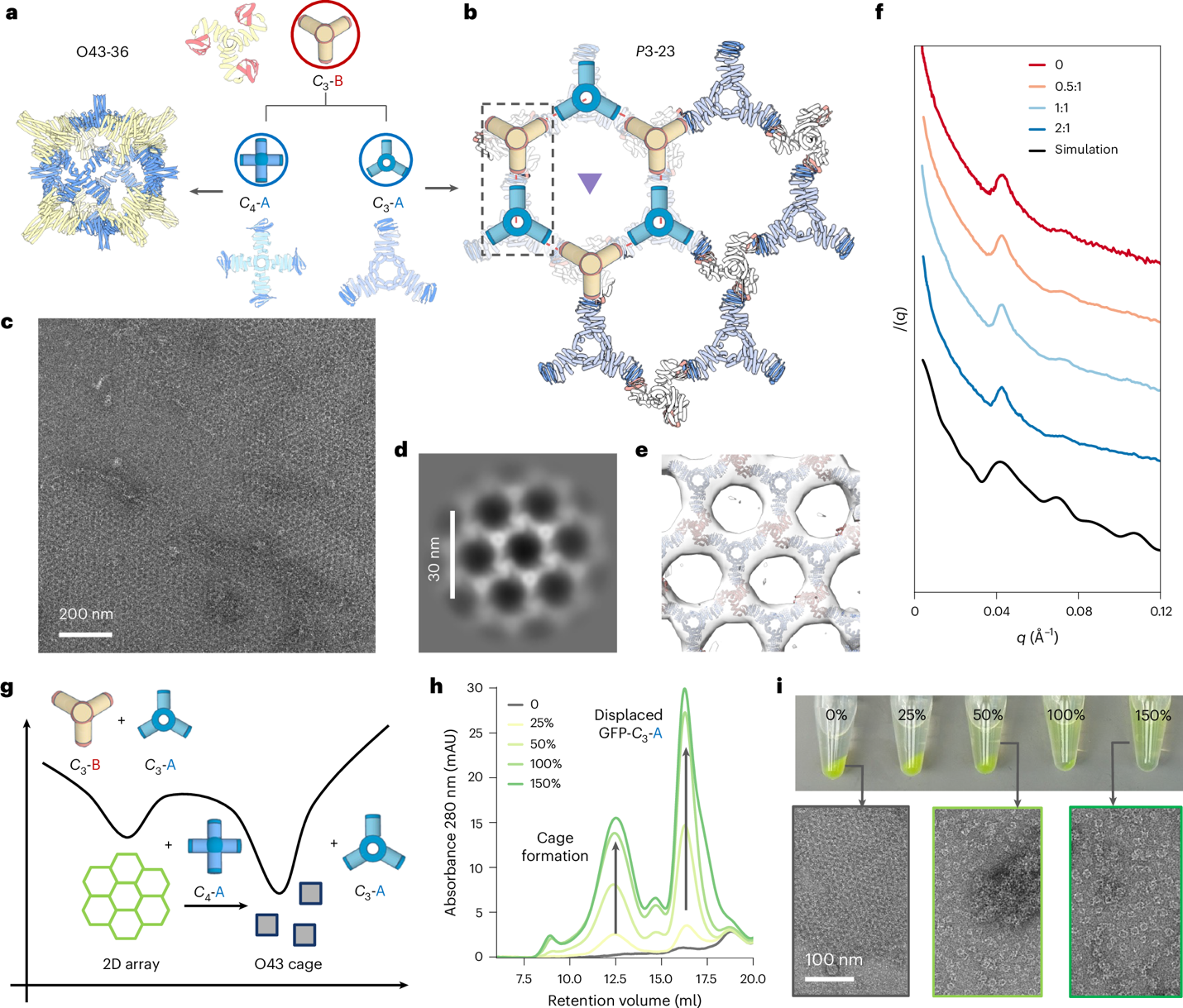
图4
4.向复杂3D 晶格迈进(图5)
设计高配位“键心”后,进一步构筑F432 立方晶格,为构建高孔隙度蛋白晶体和功能化材料提供通路。

图5
开源积木库与潜在应用
研究数据、序列与设计脚本均已开源,全球科研人员可直接下载并二次创作:
1.组件扩展:增加更多配对角度、多价连接头,嵌入多样化活性位点;2.精准医疗:开发靶向递送平台;在受损组织中响应环境变化,实时调节力学或信号特性促进修复;3.合成生物学:在活细胞内排布催化或发光组件,实现逻辑运算与信号输出,可与 DNA 纳米技术互补。
标准化之后,蛋白质自组装真正成为“纳米乐高”——尺寸缩至十亿分之一米,却同样可复用、可扩展、可重构。该工作为智能生物材料与合成生物学应用打开了全新可能。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s41563-025-02297-5