
肥胖不仅是外貌的一种体现,更是一种可导致高血压、糖尿病、心血管疾病等的代谢性疾病。肥胖还与关节炎、癌症之间也存在显著的相关性。最近的统计数据表明,肥胖是继吸烟、饮酒之后癌症的最大诱因。长期以来,研究人员一直在努力探索肥胖的治疗方案。近日,哥伦比亚大学强力教授团队和Kam W. Leong教授团队合作,发表了“正电荷定向减肥”的新发现。研究人员发现正电荷树枝状大分子聚酰胺胺(PAMAM G3,P-G3)能实现对脂肪组织的定点靶向,而且对脂肪细胞进行重新编程,从而获得更小更加健康的“小矮人”脂肪细胞。这一全新的治疗策略有望实现人们梦寐以求的“想瘦哪儿就瘦哪儿”。
相关研究成果以“Selective targeting of visceral adiposity by polycation nanomedicine”和“Polycationic PAMAM ameliorates obesity-associated chronic inflammation and focal adiposity”为题,分别于2022年12月1日和2022年11月28日发表在Nature Nanotechnology和Biomaterials期刊上。
脂肪组织在体内呈现区域分布的特点。按分布来划分,人体主要的两大脂肪组织为:围绕胃、肠等腹腔内器官的内脏脂肪组织,以及分布于浅表的皮下脂肪组织。常见的“啤酒肚”就是内脏脂肪组织过多的表现,而双下巴、手臂“拜拜肉”则是皮下脂肪过多的表现。目前临床使用的药物减肥和饮食运动干预都是全身性的,还没有针对内脏型肥胖的治疗方法。而针对皮下脂肪的治疗,如吸脂术和急性冷冻,则是属于有破坏性的物理减肥,存在相当高的安全风险和长期隐患。因此,安全有效并且能定向的减肥方法是一个迫切需要,也是减肥的理想目标。
脂肪组织中容纳和支撑脂肪细胞的细胞外基质含有大量负电荷成分。双方团队研讨后猜测这种负电基质网络有可能如高速公路系统,能够富集并把正电分子快速送抵脂肪细胞。为了验证这一猜想,研究人员将带正电的P-G3腹腔注射到肥胖小鼠体内,结果发现 P-G3 迅速富集到内脏脂肪组织内,远超过在其他组织内的水平。研究人员进一步通过改变阳离子聚合物的电荷和结构发现正电荷是靶向脂肪组织的关键因素。与P-G3结构类似的负电聚合物则完全失去了对脂肪组织的靶向性。至此,研究团队找到了靶向脂肪细胞的钥匙——正电荷。

图1:a,阳离子聚合物对脂肪组织有分布倾向性;b,小鼠腹腔注射第 3 代PAMAM阳离子聚合物(P-G3)后其在体内各器官分布示意图。
研究人员接下来出乎意料地发现正电荷P-G3具有很强的减肥效果。利用肥胖小鼠模型,研究人员发现P-G3既能预防肥胖发生,又能治疗已有肥胖。这主要归因于内脏脂肪组织的显著减少(50% -70%)。同时,P-G3处理小鼠的相关代谢功能也明显改善,包括胰岛素敏感性、葡萄糖代谢、脂代谢、全身能量代谢、慢性炎症等。因此,P-G3可以提供一种健康的减肥方法。
深入到细胞水平,成熟的脂肪细胞由前体脂肪细胞分化而来,分化后的脂肪细胞进一步合成、并储存甘油三酯等脂质成分,在机体需要时释放出来满足能量需求。令人吃惊的是,P-G3不仅没有抑制脂肪细胞生成,反而促进了前体脂肪细胞向脂肪细胞的分化,而且普遍性地抑制了参与脂质合成和存储的基因的转录表达,实现了脂肪细胞分化和其标志性脂肪合成存储功能的解耦联。P-G3是通过调节NAD+以及mTOR等营养感知信号通路实现这一解耦联的。P-G3这个独特的功能可以让新生脂肪细胞不能长大,也可以让现有的肥大脂肪细胞变小。这些又小又健康的“小矮人”脂肪细胞往往在婴幼儿和运动员中常见。在人源脂肪细胞和脂肪组织中,P-G3也表现出了相同的解耦联功能。这一发现为P-G3的临床转化提供了重要的依据。
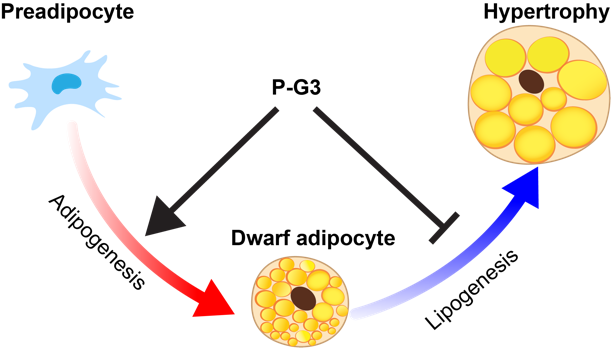
图2:P-G3将脂肪细胞的生成过程和脂质合成存储这一脂肪细胞标志性功能解耦的模式图。
研究人员对P-G3展开了进一步优化来提高应用性。一方面,在P-G3末端共价结合疏水胆固醇基团,从而让它自组装形成P-G3为壳、胆固醇链为核心的两亲性阳离子纳米颗粒。该纳米颗粒不仅保留了减肥的效果,而且对内脏脂肪的靶向性更强,也具有更好的载药能力。另一方面,利用临床常用的人血清白蛋白(HSA)为负载,构建HSA-PG3缓释纳米材料。该材料表现出很好的安全性和精准的皮下脂肪定位性。皮下脂肪局部注射HSA-PG3可以非常有效地减少局部脂肪。这一局部减肥效果是以局部脂肪组织健康重构为基础,而非破坏脂肪组织获得的。

图3:A, 皮下脂肪局部注射HSA-PG3精准定位于皮下脂肪。B, 皮下脂肪局部注射HSA-PG3有效地减少局部脂肪。
强力教授和Kam W. Leong教授团队的开创性研究工作不仅为靶向脂肪组织提供了新的方案,而且为将正电荷高分子材料和以正电荷为载体的纳米药用于治疗肥胖和其他代谢性疾病开辟了新的方向。
在这两项“姊妹”研究中,万钱芬、黄保丁和李天予博士做出了关键的贡献,并列为论文的第一作者。通讯作者是强力教授和Kam W. Leong教授。(来源:科学网)
相关论文信息:
https://doi.org/10.1038/s41565-022-01249-3
https://doi.org/10.1016/j.biomaterials.2022.121850