中国科学院上海药物研究所研究员陈小华、谭敏佳团队发展了多重光交联化学生物学策略,系统解析了Midnolin的蛋白质互作组,揭示其介导的非泛素依赖的底物降解机制,显著拓展了Midnolin的降解底物谱及潜在的可调控蛋白空间,为靶向“难成药”靶标的降解提供了新思路。3月12日,相关研究成果发表于《美国化学会志》。
蛋白质降解是细胞维持蛋白稳态、调控关键生命活动的核心过程,泛素-蛋白酶体系统与溶酶体系统是细胞内主要的蛋白降解途径。Midnolin-蛋白酶体途径是一种非泛素依赖性的蛋白降解机制,可绕过经典的泛素化过程,直接招募底物至蛋白酶体进行降解,展现靶向传统“难成药”靶标的巨大潜力。由于Midnolin与其互作蛋白之间往往是动态或微弱的相互作用,现有方法难以全面、精确地发现其完整的互作组,极大地限制了对Midnolin功能多样性的理解及其治疗潜力的挖掘。
在前期研究基础上,研究团队构建了一种高效的多重光交联平台,能高灵敏、有效地揭示Midnolin的蛋白质互作组。研究团队一方面,采用具有赖氨酸选择性的光交联剂,实现对Midnolin互作蛋白的精准捕获;另一方面通过基因密码子扩展技术,将具有光交联活性的非天然氨基酸定点引入到Midnolin的Catch结构域中,在光激活下实现活细胞内Midnolin与互作蛋白的共价捕获。
基于此平台,研究团队成功鉴定出一批Midnolin的互作蛋白,显著扩展了Midnolin已知的互作蛋白谱。研究团队首次发现并验证了4个新的Midnolin降解底物,ETV3、JUN、PRKD1和FN3KRP。值得注意的是,这些新底物是现有基于蛋白质稳定性的荧光筛选方法无法检测到的。
研究团队进一步分析发现,Midnolin能够介导转录因子JUN蛋白的非泛素依赖的蛋白酶体途径降解,提示通过Midnolin介导JUN降解在疾病治疗中的潜力。研究团队同时发现多个Midnolin的非降解互作蛋白,揭示了Midnolin在降解之外调控底物蛋白的其他细胞功能。
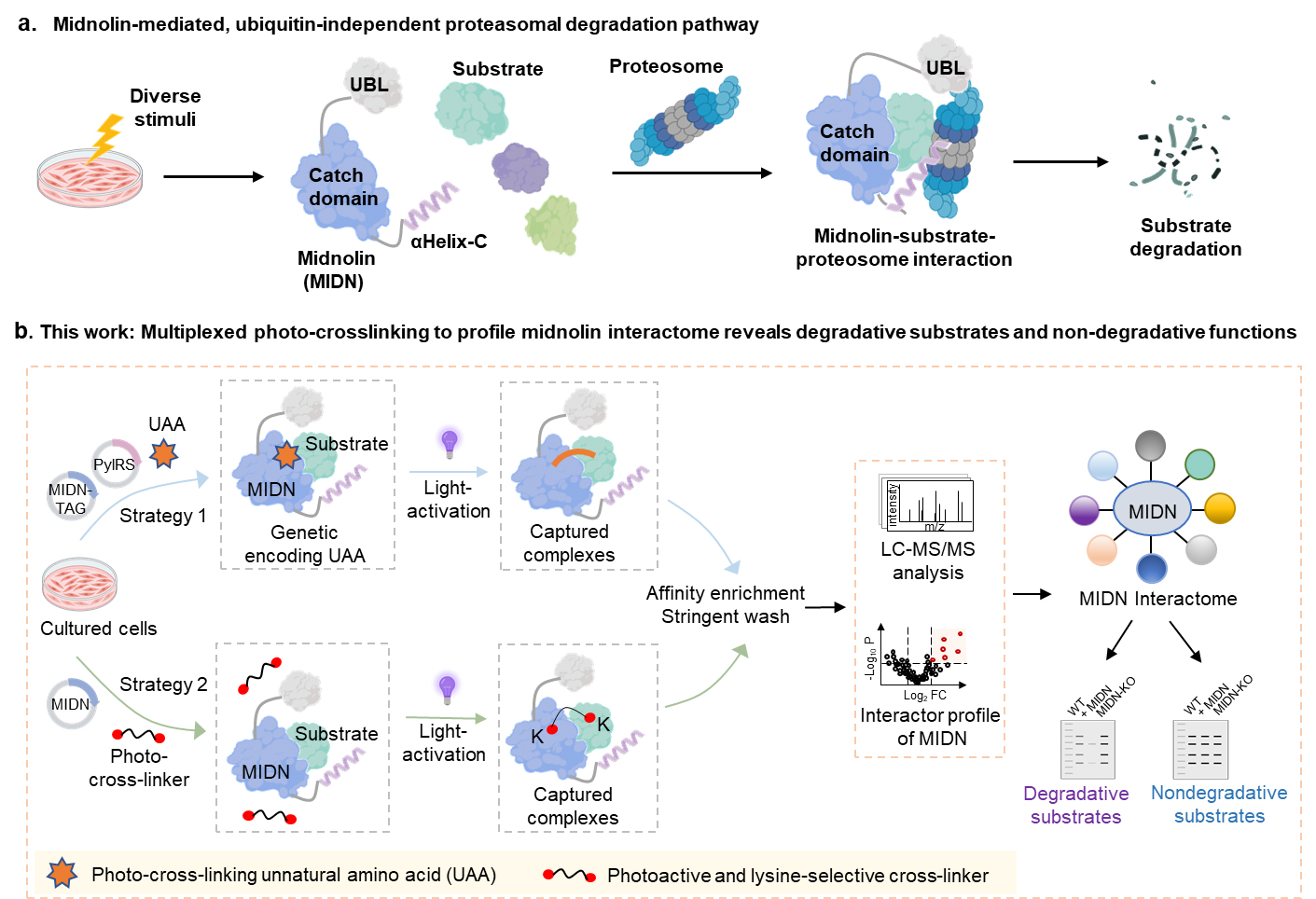 多重光交联化学生物学策略揭示Midnolin蛋白质互作组及其介导的非泛素依赖降解底物。研究团队供图
多重光交联化学生物学策略揭示Midnolin蛋白质互作组及其介导的非泛素依赖降解底物。研究团队供图
相关论文信息:https://doi.org/10.1021/jacs.5c22099
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。