|
|
|
|
|
给视神经细胞披上“隐形衣”:研究揭示视神经保护新思路 |
|
|
近日,中山大学中山眼科中心教授李轶擎/卓业鸿团队成功揭示了唾液酸化在视网膜神经节细胞(RGC)存活与轴突再生中的关键作用。该研究表明,靶向提高RGC的唾液酸化水平,能够促使小胶质细胞向稳态表型转变,显著提升非αRGC的存活率,并促进其轴突再生,为基于糖基化修饰调控的视神经保护策略提供了崭新的见解。相关研究成果发表于《神经炎症杂志》。
青光眼是全球主要的不可逆致盲眼病之一,早期往往没有明显症状,但一旦发病,视神经——这条连接眼睛和大脑的“信息高速公路”——便会逐渐受损,最终导致视力丧失。遗憾的是,视神经损伤后几乎无法自行再生,这也是青光眼等视神经损伤性疾病难以治愈的核心原因。RGC是眼睛里至关重要的神经细胞,是视觉信号由眼睛传递至脑的唯一输出通路。有趣的是,RGC并非一种“统一”的细胞,它们具有高度异质性。不同亚型的RGC在遭受损伤后,展现出截然不同的存活能力。其中,αRGC展现出较强的抗损伤能力和再生能力,深入理解这些细胞为何如此“顽强”,对于开发其他亚型RGC的保护策略至关重要。
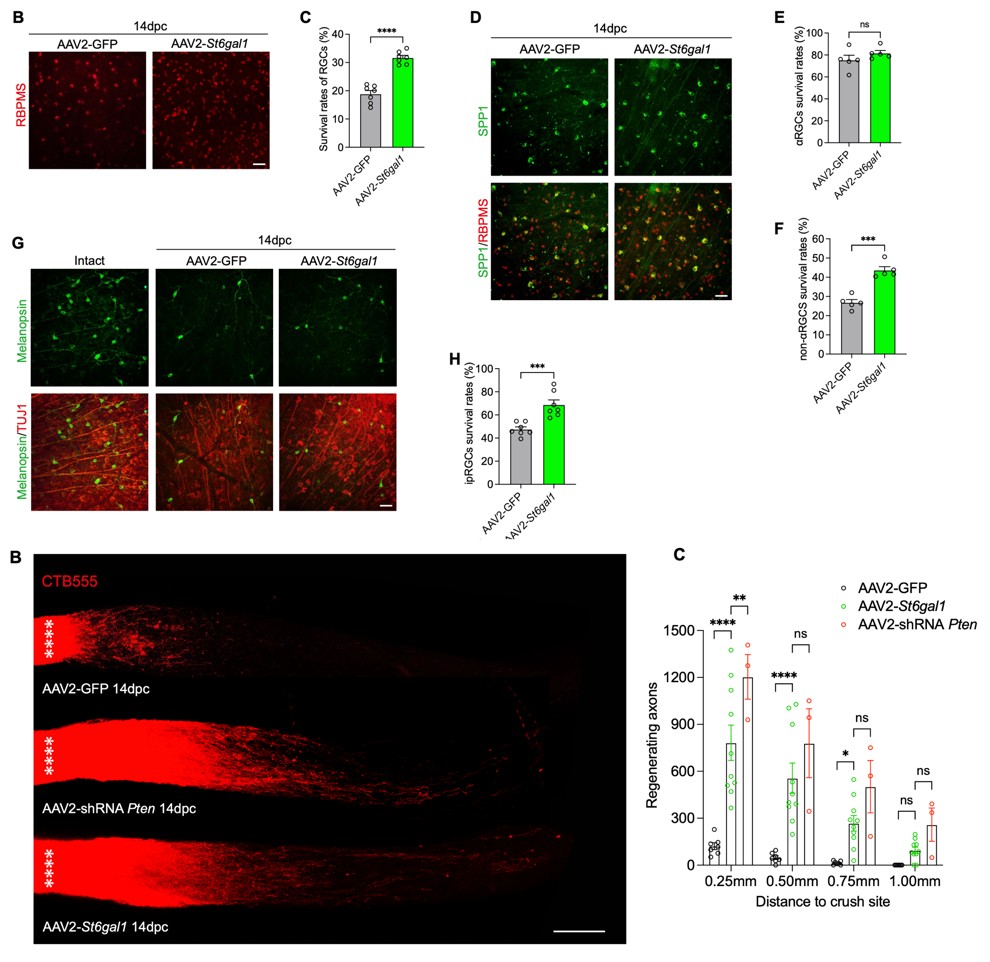 过表达St6gal1增强唾液酸化提高non-αRGC存活率及促进轴突再生。研究团队供图
过表达St6gal1增强唾液酸化提高non-αRGC存活率及促进轴突再生。研究团队供图
在神经系统中,小胶质细胞承担着“清道夫”的角色。当神经元死亡后,它们会及时清除残骸,维持环境稳定。但问题在于,有些神经元在受损后虽处于应激状态,但尚未真正死亡,却可能被小胶质细胞提前“吞噬”,这种现象被称为“吞噬性死亡”。在视神经损伤中,小胶质细胞的作用可谓“敌友难分”。它们履行清道夫职责,及时清除已经死亡的RGC;然而,这种吞噬也可能变得“不分青红皂白”,将邻近仍有存活能力的RGC一并吞噬,反而加剧了神经元的丧失,推动疾病进展。
研究发现,小胶质细胞的这种吞噬行为受细胞表面“Eat me”(促吞噬)与“Don’t eat me”(抗吞噬)信号的精确调控。其中,关键的抗吞噬信号之一,便来自神经元表面的唾液酸修饰,它像一层“隐形衣”,帮助神经元避免被小胶质细胞误伤。唾液酸化是一种由唾液酸转移酶介导的关键翻译后修饰过程,该过程催化唾液酸添加至糖蛋白末端,进而调节细胞间的相互作用以及免疫逃逸。研究团队推测,αRGC较高的存活率可能源于其对小胶质细胞清除的抵抗能力,这种抵抗或许是通过增强“Don’t eat me”信号,使这些神经元不易受到活化小胶质细胞的攻击和吞噬。
深入研究发现,在视神经损伤后,视网膜唾液酸转移酶ST6Gal1的表达以及介导的α2,6-唾液酸化水平整体下降。然而,与其他亚型相比,αRGC却能够在损伤应激下相对稳定地维持较高水平的 ST6Gal1 表达。进一步实验表明,正是这种持续的高唾液酸化状态,构成了αRGC在逆境中更具“韧性”的重要分子基础,是其生存优势的关键因素之一。
在此基础上,研究团队利用腺相关病毒在整体RGC中调控唾液酸化水平。结果显示,当唾液酸化水平被提高后,原本更为脆弱的non-αRGC存活率显著上升,其抗损伤能力明显增强。与此同时,高唾液酸化状态还能调节小胶质细胞由活化、吞噬倾向向稳态表型转变,从而减少其对受损但仍可存活RGC的过度吞噬,并显著促进视神经轴突再生。
该研究不仅揭示了视神经损伤后ST6Gal1的动态变化规律,更从机制层面解释了αRGC为何“更耐受”——其背后依赖的是更强的唾液酸化保护屏障。通过增强唾液酸化能够缩小RGC亚型之间的生存差异,并在多种模拟青光眼的损伤模型中展现出广泛的神经保护作用,并显著促进视神经再生。这一发现为基于糖基化调控的视神经保护策略提供了新的理论依据,并为青光眼等视神经损伤性眼病的治疗开辟了新的方向。
相关论文信息:https://doi.org/10.1186/s12974-026-03736-z
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。