近日,华南理工大学医学院副教授王卓团队携手浙江大学、南方医科大学等科研人员,首次揭示了社交隔离会触发大脑特定区域的“铁聚积”现象,进而激活一条全新的神经可塑性通路。研究团队将这一机制命名为“铁可塑性”。相关研究成果近日发表于《细胞-代谢》杂志。
“该发现不仅破解了‘孤独伤脑’这一长期存在的谜题,更为开发无需传统抗焦虑药物、无创且可逆的全新干预方法开辟了道路。”论文第一作者兼通讯作者王卓指出,该研究融合了神经科学、金属生物学代谢调控与转化医学等多个领域的知识,真正实现了“从实验室到病床前”的全链条创新。
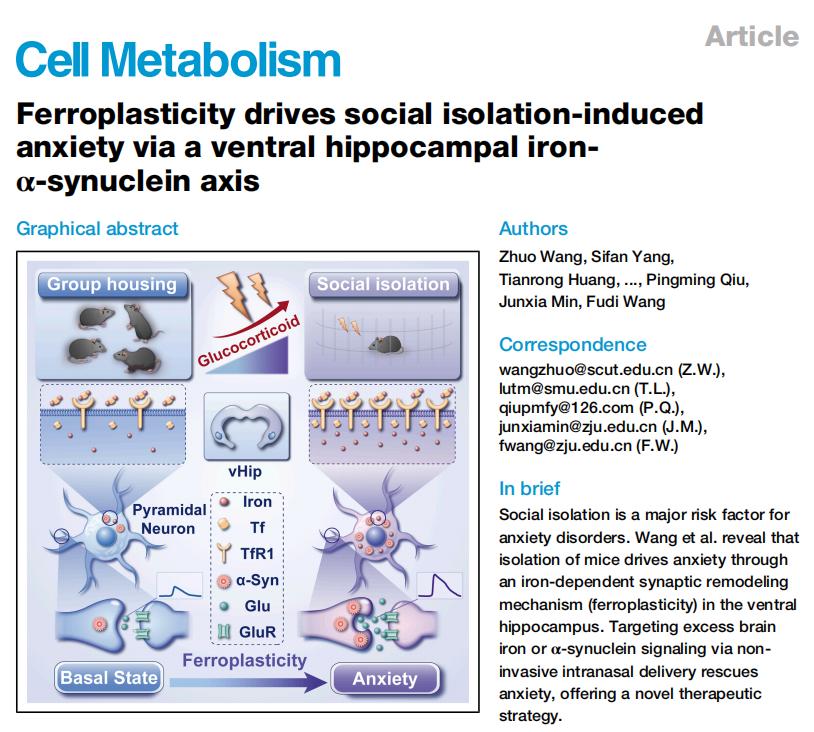 研究思路示意图。研究团队供图,下同
研究思路示意图。研究团队供图,下同
在日常生活中,不少人都有过这样的感受:长时间独处后,即便没有发生任何特别的事情,也会莫名地感到心慌、坐立不安,甚至对社交产生恐惧。长期以来,科学家们也一直在探寻,为何“孤独”会引发焦虑?其背后的生物学机制究竟是什么?实际上,社交隔离并非仅仅影响心情,它还在悄然改变着我们的大脑。
研究团队通过构建模拟人类长期独居的小鼠模型展开研究。他们发现,被单独饲养的小鼠大脑中一个名为“腹侧海马”的区域(该区域是更侧重于调控情绪的海马亚区)铁含量出现异常升高。可别小瞧这多出来的铁,它并非有益的“补品”。
过量的铁就如同一个“错误信号”,会激活一种名为α-突触核蛋白(α-Syn)的分子,导致神经元过度放电。这一过程就如同电路短路一般,不断向身体发送“危险!快逃!”的焦虑警报。更为关键的是,这种变化精准地作用于情绪中枢,使得大脑对“社交剥夺”产生高度特异的应激反应。
过去,人们普遍认为铁只是维持神经健康的“营养元素”。然而,该研究却证明,在心理压力的作用下,铁会成为一把“双刃剑”。它能够直接驱动神经突触的结构与功能发生重塑。研究团队将这一全新机制命名为“铁可塑性”,其含义为“由铁介导的、依赖经历的神经可塑性”。这一命名将脑内铁代谢紊乱与情感障碍直接关联起来,为理解精神疾病的代谢根源打开了一扇新的大门。
研究团队尝试采用鼻腔给药(这种方式具有无创且能直达大脑的优势)的方式,针对铁可塑性中的关键分子铁或者α-突触核蛋白进行干预。实验结果令人振奋:仅仅经过2周的治疗,小鼠的焦虑行为便显著减轻,神经元活动也恢复正常。而且,这种治疗效果甚至比让小鼠重新回到群体生活(“再社会化”需要4周时间)还要快。
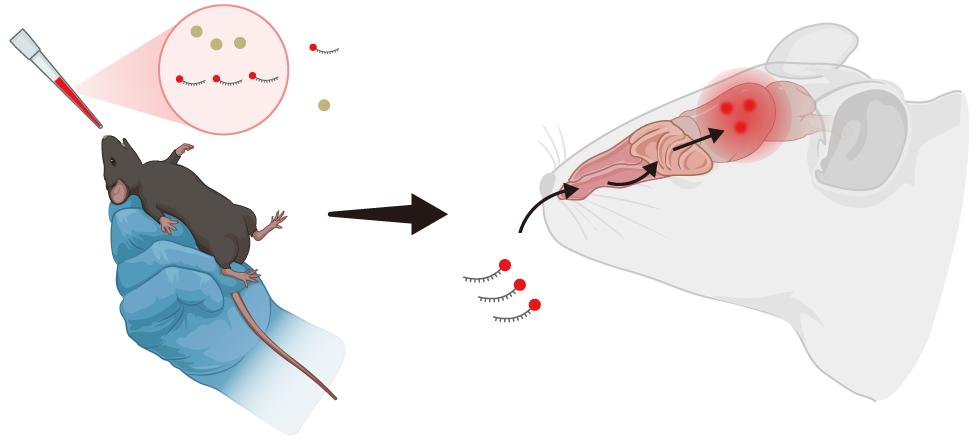 鼻腔给药示意图。
鼻腔给药示意图。
这一发现意味着,未来或许只需一支“鼻喷剂”,就能够为独居老人、封闭岗位工作者、术后隔离患者、青少年社交回避者等社交隔离相关心理问题的高风险人群,提供一种安全、便捷的预防或缓解焦虑的方法。
据估算,全球有超过10亿人受到社交隔离相关心理问题的困扰,这些人都有可能从这一机制的研究成果中获益。这为未来开发非侵入性、靶向明确的抗焦虑疗法提供了全新的思路。
“解决社交隔离引起的孤独问题,是应对现代公众卫生健康工作、实现健康中国、幸福广东目标的内在要求。”王卓表示,下一步,团队将开展多方面的工作:推进鼻喷制剂的人体安全性与剂量优化开发;研发无创检测腹侧海马铁沉积的影像技术(例如高场MRI);探索相关机制在其他神经精神疾病发生中的作用等。
相关论文信息: https://doi.org/10.1016/j.cmet.2025.12.022
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。