|
|
|
|
|
揭开光合作用“跷跷板”的秘密 |
|
中日科学家成功解析绿藻光合作用状态转换调控的超分子结构基础 |
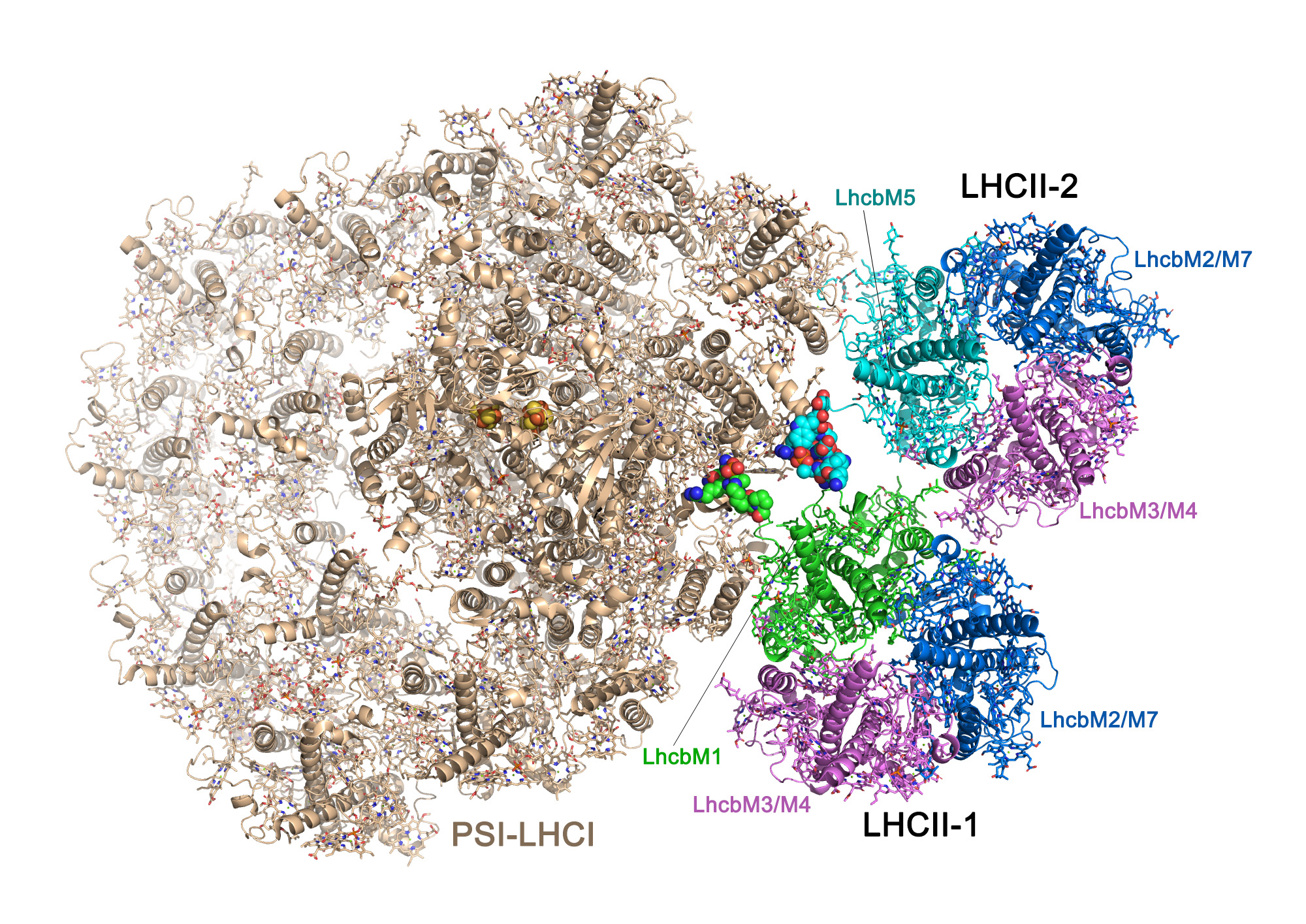
衣藻PSI-LHCI-LHCII超复合物的总体三维结构图(课题组供图)
在藻类和绿色植物中,存在光系统I(PSI)和光系统II(PSII)。它们的外周天线——捕光复合物I和II(LHCI和LHCII)能吸收光能并将能量传递给两个光系统,进而驱动光合作用电子传递和能量转换过程。
中科院生物物理所李梅课题组、柳振峰课题组联合日本国立基础生物学研究所Minagawa教授课题组,合作攻关解析了莱茵衣藻PSI-LHCI-LHCII超复合物的高分辨率冷冻电镜结构。相关论文于7月8日发表在《自然—植物》。
“在藻类和植物的光合作用中,存在一种类似于跷跷板的分子动态过程,被称为状态转换调控。”论文通讯作者之一李梅对《中国科学报》说,“这种机制能调节捕光天线向两个光系统分配能量,使得二者的激发水平处于相对平衡的状态。”
当PSII被过度激发时,绿藻和植物PSII的捕光复合物LHCII被磷酸化,部分磷酸化LHCII三体与PSII解离并与PSI结合形成PSI-LHCI-LHCII超复合物,从而增加向PSI反应中心传递的能量,实现了激发能在PSII和PSI之间的平衡分配——这种“跷跷板”作用能帮助藻类和植物适应自然界多变的光照条件,提高光合作用效率。
绿藻中的PSI-LHCI-LHCII超复合物比植物中相应的复合物更大更复杂,包含至少2个LHCII三体。在莱茵衣藻(一种单细胞模式绿藻)中,9个不同的LhcbM蛋白参与形成不同组成的LHCII三聚体。
“因此,莱茵衣藻PSI-LHCI-LHCII超复合物的结构和组成极为复杂,具体是由哪种LhcbM蛋白参与介导LHCII与PSI-LHCI复合物装配的问题一直以来都不清楚,其能量传递途径也有待研究。”另一位论文通讯作者柳振峰说。
此次研究人员成功解析了莱茵衣藻PSI-LHCI-LHCII超复合物的高分辨率冷冻电镜结构。发现该超分子复合体是由PSI核心在一侧结合8个LHCI蛋白,在另一侧结合2个LHCI单体和2个磷酸化LHCII三聚体,构成一个总分子量达~1100 kDa的膜蛋白-色素复合体。
基于高质量电镜密度图,研究人员准确指认了参与构成该超复合物的磷酸化LHCII中全部LhcbM蛋白,发现LhcbM1和LhcbM5通过它们的磷酸化氨基末端区域直接与PSI核心相互作用,且LhcbM5还介导并稳定了PSI核心与LhcbM1之间的装配。此外,对分别缺失LhcbM1(DLhcbM1)和LhcbM5(DLhcbM5)的衣藻突变株的生化、功能和结构研究结果表明,LhcbM5对于超复合体的形成是必不可少的,DLhcbM5突变株的状态转换明显受到影响。在DLhcbM1突变体中,LhcbM3蛋白取代了LhcbM1与PSI结合,因而DLhcbM1突变体中仍然能够形成PSI-LHCI-LHCII超复合物。
“该项研究的亮点在于发现绿藻中一个特定的捕光蛋白LhcbM5参与捕光复合物LHCII与光系统I的装配,并在状态转换中发挥重要的作用。这对于我们深入理解不同亚型的捕光蛋白在光合作用及其调节过程中的特定生物学功能具有重要的意义。”李梅说。
“植物和藻类光合作用调控机理是一个令人兴奋的前沿研究方向,此次研究中,中日两国的3个科研团队互相配合、取长补短,通过结构生物学、生物化学和分子遗传学等多种方法相结合,才得以发现并深入探讨特定类型捕光蛋白在光合作用状态转换过程中的作用机制。”柳振峰表示。
相关论文信息:https://doi.org/10.1038/s41477-021-00960-8
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。