|
|
|
|
|
研究揭示STUB1-VCP/p97轴调控线粒体自噬机制 |
|
|
近日,中山大学中山医学院副教授卢广团队与挪威奥斯陆大学教授方飞团队合作,研究揭示了一条不依赖PARL蛋白酶切割的全长PINK1降解新通路,阐明了STUB1-VCP/p97轴通过精确调控PINK1蛋白水平维持线粒体稳态的分子机制。相关研究成果发表于《细胞报告》(Cell Reports)。
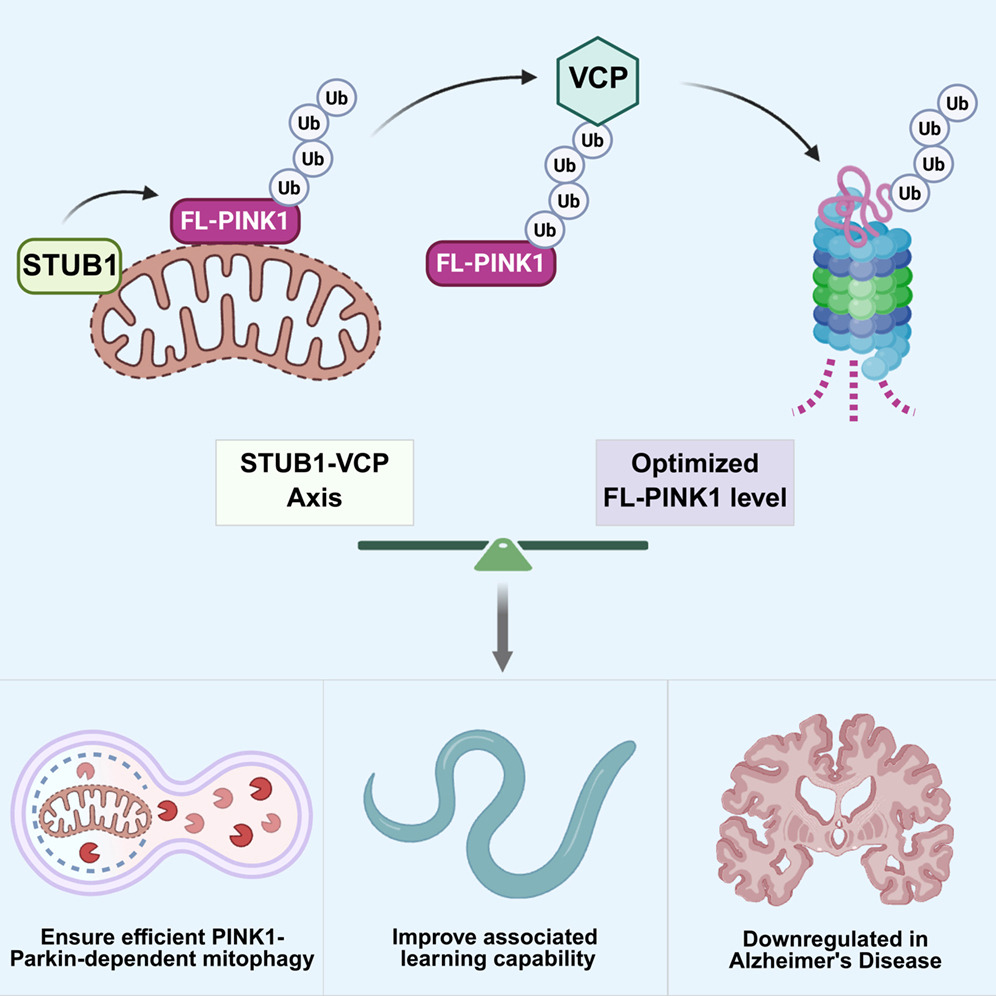
相关研究示意图。研究团队供图
研究团队利用经典线粒体损伤模型证实,损伤后期的全长PINK1主要经由泛素-蛋白酶体系统降解,且该过程不依赖传统的PARL蛋白酶切割。通过SILAC定量蛋白质组学技术,团队筛选并验证了泛素E3连接酶STUB1与AAA+ ATP酶VCP/p97是调控全长PINK1蛋白稳定性的关键分子:STUB1催化全长PINK1发生K48连接型泛素化修饰,随后VCP/p97复合物识别并提取泛素化的PINK1,将其递送至蛋白酶体降解。
进一步研究发现,STUB1-VCP/p97轴功能受阻会导致全长PINK1异常积累,这不仅未能增强线粒体自噬,反而对其产生抑制作用。在分子机制层面,过量PINK1过度激活Parkin蛋白,加速其自身泛素化降解,导致受损线粒体表面泛素化信号不足及关键自噬受体OPTN、NDP52招募缺陷,最终阻碍损伤线粒体的清除。
该调控轴的生理与病理意义在多个层面得到验证:细胞水平上,其缺失可引发线粒体形态和功能异常;阿尔茨海默病患者海马脑区中,STUB1、VCP/p97及Parkin蛋白水平均显著下调;秀丽隐杆线虫模型中,该轴的缺失可导致神经元线粒体自噬缺陷及联想学习记忆能力受损。
该研究为理解线粒体质量控制机制提供了新视角,也为神经退行性疾病的干预提供了潜在靶点。
相关论文信息:https://doi.org/10.1016/j.celrep.2026.117183
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。