|
|
|
|
|
双向切割策略有效提升CRISPR介导的同源定向修复效率 |
|
|
华东理工大学副教授周胜敏团队系统阐明了限制CRISPR精准敲入效率的关键DNA修复机制,并提出了一种具有普适性的高效同源重组设计策略,为基因编辑中插入位点依赖性强、目标片段难以高效敲入的问题提供了可预测、可推广的解决方案。相关研究成果近日发表于《核酸研究》。
CRISPR-Cas9是当前最重要的基因组编辑技术之一,可在单链向导RNA(sgRNA)的引导下,在基因组特定位点进行切割,使得DNA双链断裂,并借助细胞内DNA修复通路实现基因改造。在生物体内,外源序列的精准插入通常依赖同源定向修复(HDR)过程。然而,在真菌等体系中,HDR效率常受到切割位点位置、插入片段长度以及修复通路竞争等多重因素制约,导致部分插入位点长期存在“难以敲入”的问题。
研究团队从DNA修复过程中的空间几何约束出发,发现供体DNA与染色体链侵入路径之间的几何错位,是导致HDR介导精准敲入效率下降的关键原因。研究团队解析了同源重组相关蛋白在双链断裂周围的方向性加载规律,明确了有效修复窗口的空间特征。
在此基础上,研究团队提出了双向切割形成几何对齐窗口的设计策略。具体而言,通过在目标位点两侧引入成对的sgRNA进行切割,实现供体同源臂与内源DNA修复路径的空间匹配,从而稳定提升精准敲入效率。
系列实验结果表明,该策略在不同插入片段长度及多类编辑任务中均表现出良好适用性,并可推广应用。
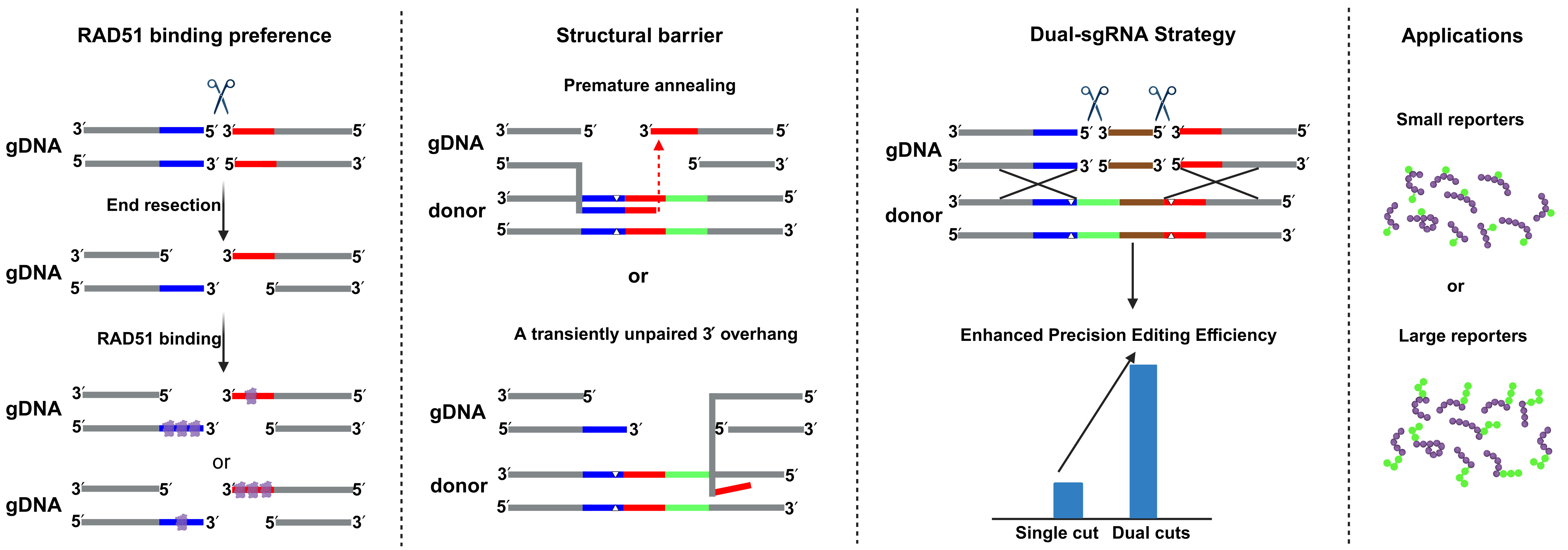 CRISPR精准敲入的结构性限制及双sgRNA提升效率的原理示意。研究团队供图
CRISPR精准敲入的结构性限制及双sgRNA提升效率的原理示意。研究团队供图
相关论文信息:https://doi.org/10.1093/nar/gkag095
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。