3月5日,南方医科大学南方医院教授吴德华、刘莉、董忠谊团队的一项重要研究成果发表于《自然-癌症》(Nature Cancer),成功揭示免疫治疗疗效毒性“解偶联”新靶点,为肿瘤免疫治疗带来新希望。
论文最后通讯作者董忠谊指出,该研究首次发现了导致免疫治疗多器官不良反应的全新靶点,并据此提出通过干预该靶点,实现免疫治疗“减毒性不减疗效”的精准毒性管理策略。这一成果有望打破当前临床中免疫相关不良事件(irAEs)“被动应对”以及“以牺牲疗效为代价”的防治困境,为肿瘤患者接受免疫治疗提供更安全、有效的保障。
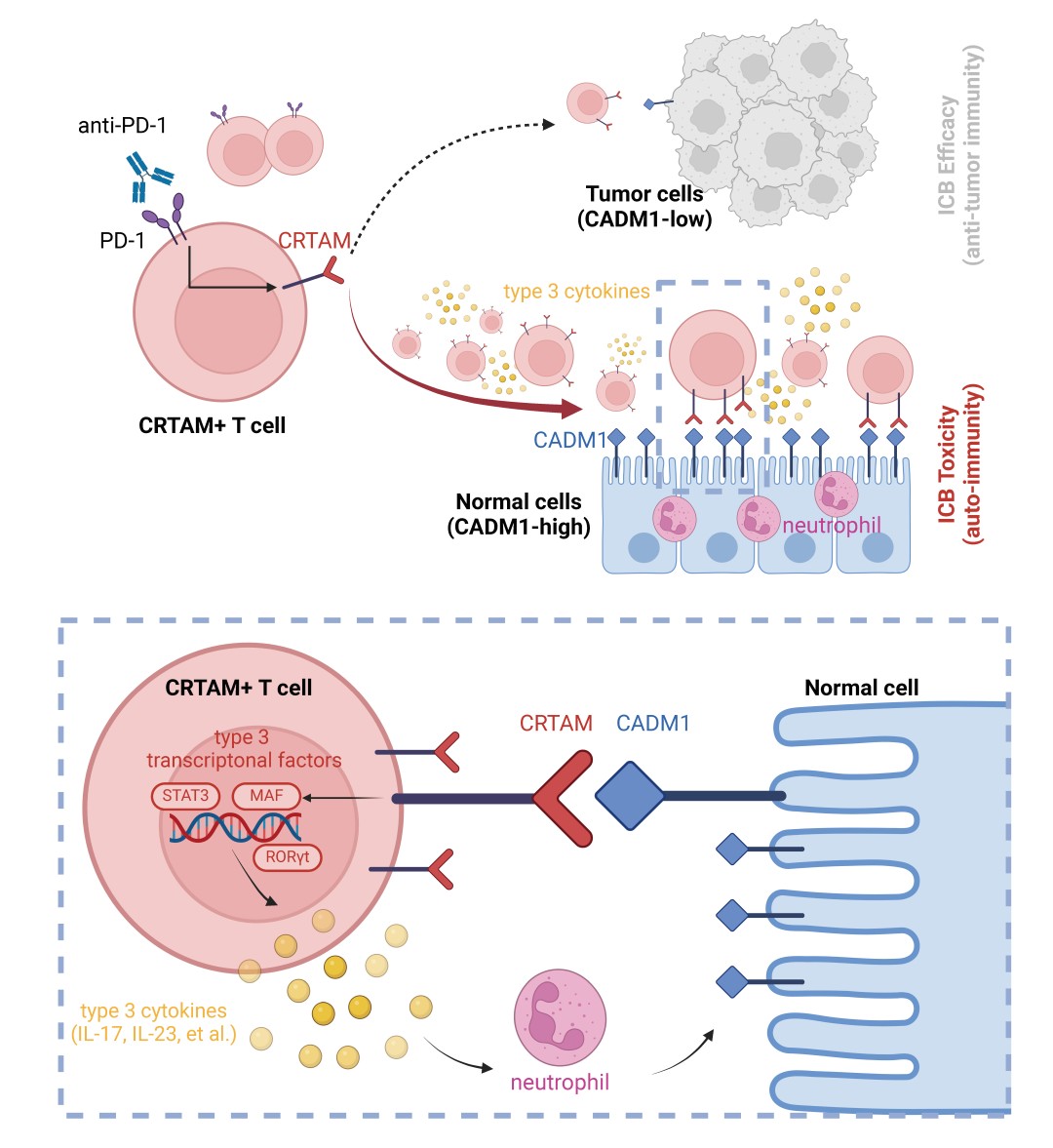 CRTAM调控免疫不良反应机制图。研究团队供图
CRTAM调控免疫不良反应机制图。研究团队供图
免疫检查点阻断疗法堪称免疫细胞的“兴奋剂”,能为免疫细胞在抗癌战斗中提供源源不断的动力。然而,过度兴奋的免疫细胞常常“失控”,在摧毁肿瘤细胞的同时,也可能误伤人体正常组织。据统计,高达20%-30%的患者会遭遇免疫相关不良事件。这种由免疫细胞误伤正常组织引发的状况,轻则导致治疗中断,重则危及患者生命。
目前,针对irAEs的管理策略主要以糖皮质激素的“免疫抑制”能力为代表。虽然糖皮质激素能有效抑制irAEs,但也会削弱免疫细胞的抗肿瘤能力,让临床医生在平衡疗效和安全性时陷入两难境地。因此,以实现“免疫治疗疗效与毒性解偶联”为目标,探寻介导irAEs却不影响治疗疗效的毒性特异性分子,从根源上阻止irAE的发生发展,达到“减毒性不减疗效”的目的,具有重要的临床意义。
面对这一临床挑战,研究团队大胆创新,通过多组学数据构建了“免疫治疗疗效-毒性解偶联模型”。从模型中的“毒性特异性基因”里,筛选出了irAEs的关键靶点CRTAM,并通过构建多种irAEs动物模型进行了全面验证。
在分子机制层面,团队发现CRTAM+ T细胞能够结合正常组织表达的配体CADM1,这使得它们更倾向于浸润正常组织而非肿瘤组织。同时,CRTAM+ T细胞会激活以IL-23为核心的3型免疫反应,进而介导正常组织的炎症损伤。
在临床转化方面,团队自主研发了抗CRTAM单克隆抗体,并证实靶向CRTAM可以在不损害抗肿瘤免疫的前提下,有效减轻免疫治疗相关的多种器官不良反应。此外,团队通过临床队列验证了血液活检检测“CTRAM-III型免疫”轴的可行性。
该研究成果有望为irAEs管理提供从“被动干预”迈向“主动预防”的新策略,推动肿瘤免疫治疗向更安全、更精准的方向发展。
相关论文信息:https://doi.org/10.1038/s43018-026-01135-0
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。