中国科学院动物研究所研究员刘光慧、曲静联合国家生物信息中心研究员张维绮、四川大学华西医院教授杨家印,首次从蛋白质时空维度,系统解析了人体器官衰老的显著异质性及其动态架构。近日,相关研究发表于《细胞》。
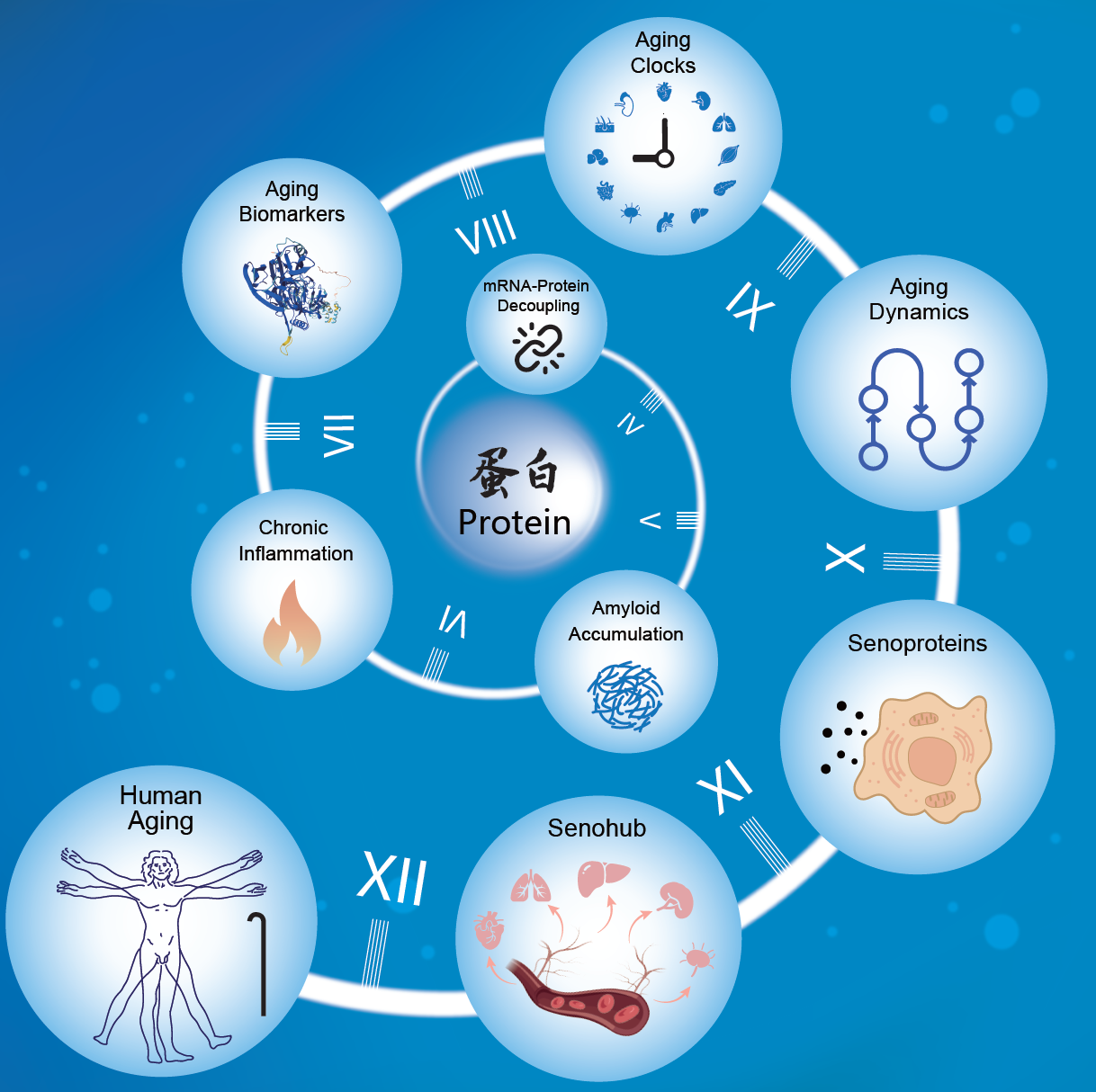 研究示意图
研究示意图
?
衰老的深层分子机制是生命科学领域悬而未决的核心命题。而蛋白质稳态的失衡是衰老进程中标志性的分子特征之一。因此,系统绘制跨越生命周期的蛋白质组动态全景图谱,解析器官及系统尺度下蛋白质网络的重编程规律,对于识别衰老的核心驱动因素并确立干预靶标具有重要意义。
基于前沿人工智能算法,研究团队构建了覆盖13种人类组织的特异性“蛋白质组衰老时钟”。深度分析揭示:30岁左右为衰老轨迹的初始分水岭,肾上腺组织率先呈现衰老特征,同期主动脉亦出现稳态偏移。45-55岁为衰老进程的里程碑式转折点,绝大多数器官蛋白质组在此阶段经历“分子级联风暴”,差异表达蛋白呈爆发性激增。值得注意的是,主动脉蛋白质组在此过程中的重塑最为剧烈,其分泌组与循环血浆蛋白质组动态谱呈现强共演变特征,提示衰老相关分泌因子可能是介导衰老信号系统性传播的枢纽机制。
团队锁定关键分泌因子展开功能解析。代表性范例GAS6在衰老主动脉组织及循环系统中呈现跨尺度显著富集;体外功能研究证实,GAS6可直接驱动人类血管内皮细胞与平滑肌细胞衰老表型。类似地,GPNMB、COMP、HTRA1、IGFBP7等衰老相关分泌因子亦被证实可直接诱导血管细胞衰老。这些结果确证了“衰老扩散”理论的核心原则——即局部衰老组织通过特异性分泌因子驱动远端器官衰老级联,从而将衰老研究的范式从聚焦传统的“细胞内分子机制”拓展至“器官间通讯网络”的系统维度。
相关论文信息:https://doi.org/10.1016/j.cell.2025.06.047
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。