|
|
|
|
|
海洋链霉菌吲哚生物碱和多环内酰胺生物合成机制获揭示 |
|
|
近日,中国科学院南海海洋研究所研究员张长生团队在海洋链霉菌来源吲哚生物碱类和多环内酰胺类活性次级代谢产物的生物合成机制解析方面取得新进展。相关成果分别发表于《有机化学通讯》(Organic Letter)和《中国化学》(Chinese Journal of Chemistry),并均被选为封面文章。
海洋微生物在适应高盐、高压、黑暗、低温(或局部高温)、寡营养等严酷的生存环境压力下,进化出了与之相适应的生理生化特征或特殊的代谢途径,因此可产生化学结构复杂或生物活性独特的次级代谢产物,对这些产物的生物合成机制进行深入研究可为其结构改造和绿色生物制造提供重要理论依据。
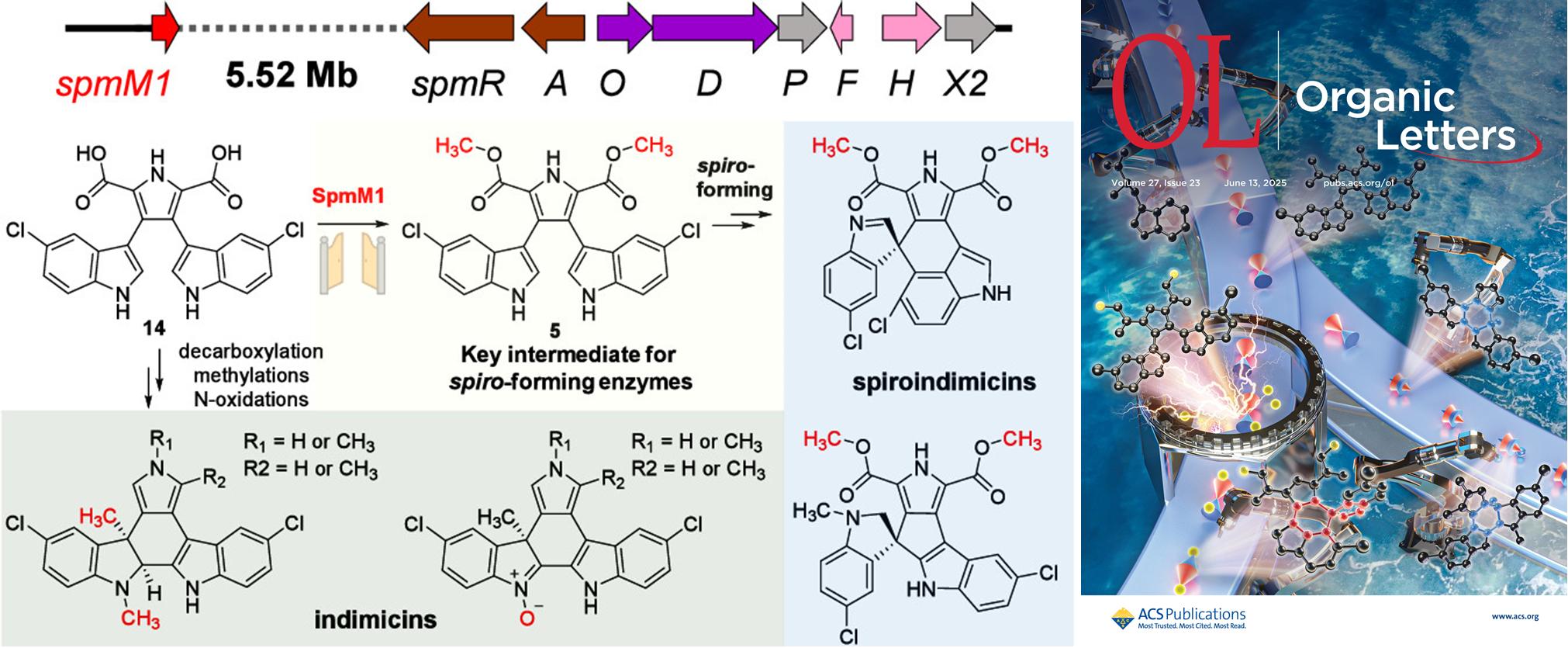 色氨酸二聚体生物合成途径中游离甲基转移酶SpmM1的功能研究。研究团队供图,下同
色氨酸二聚体生物合成途径中游离甲基转移酶SpmM1的功能研究。研究团队供图,下同
?
细菌来源色氨酸二聚体是一类具有显著生物活性的天然产物,其中midostaurin已被FDA批准用于治疗白血病。研究团队前期从深海来源链霉菌Streptomyces marincola SCSIO 03032中发现了3类具有细胞毒活性的色氨酸二聚体,克隆鉴定了参与色氨酸二聚体的生物合成基因簇(spm),证实spm为非典型基因簇,即在基因簇外存在游离的生物合成基因。
研究团队在国家重点研发计划、国家自然科学基金等项目的资助下,成功从菌株SCSIO 03032基因组中鉴定了一个游离在spm基因簇外的甲基转移酶SpmM1,从其突变株中分离获得了5个新颖的色氨酸二聚体IDMs,通过生化表征确定SpmM1负责催化LNMs中吡咯环侧链羧基的氧甲基化,进一步结合喂养实验证实SpmM1通过甲基化反应控制SPMs和IDMs生物合成途径的分化,且羧甲基为SPMs形成的特异识别位点。以上结果为鉴定其它游离在基因簇外的后修饰酶提供了研究思路。
多环内酰胺类天然产物具有复杂的化学结构和良好的生物活性,是药物先导化合物和生物农药的重要资源。多环内酰胺类天然产物的化学合成步骤多、收率低,但生物合成却非常简洁和保守,可通过途径改造实现不同类型多环内酰胺类天然产物的绿色定制生产。遗憾的是,目前仍缺少高效、干净的底盘宿主应用于多环内酰胺类天然产物基因簇的异源表达,且尚不清楚数量最多的5/5型和5/5/6型多环内酰胺类天然产物结构中C14位氧化修饰差异的生物合成机制。
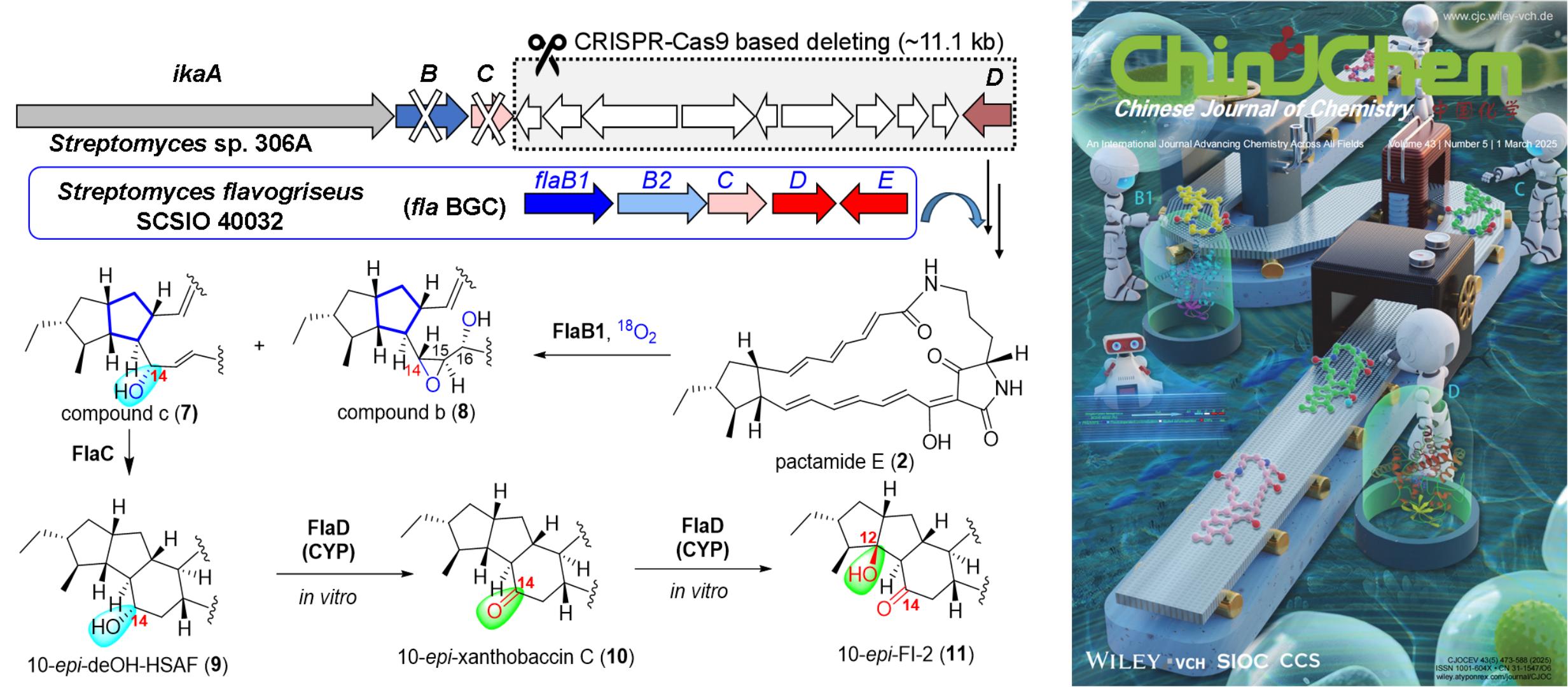 PoTeMs异源表达底盘细胞306A构建及C14位迭代氧化机制解析。
PoTeMs异源表达底盘细胞306A构建及C14位迭代氧化机制解析。
?
研究团队通过大片段敲除改造海洋链霉菌Streptomyces sp. ZJ306,构建了专属生产多环内酰胺类天然产物多烯前体的干净底盘细胞306A,为实现多环内酰胺类天然产物生物合成基因“即插即用”和药源多环内酰胺类天然产物的结构多样化奠定了基础。
团队进一步通过在底盘细胞306A中的组合生物合成比较研究表征了南海来源放线菌Streptomyces falvogriseus SCSIO 40032中沉默多环内酰胺类天然产物基因簇fla的生物合成途径,通过喂养和同位素标记实验证实黄素环化酶FlaB1在催化C6-C13环化的同时引入羟化和环氧化修饰,体外实验进一步确定P450酶FlaD及其同源酶FtdF、SSHG-05717负责将5/5/6型多环内酰胺类天然产物中的C14位羟基转化为酮基,同时催化后续的C12位羟化。该研究成功揭示了5/5型和5/5/6型多环内酰胺类天然产物中C14位迭代氧化修饰的生物合成逻辑。
相关论文信息:https://doi.org/10.1021/acs.orglett.5c01012
https://doi.org/10.1002/cjoc.202400982
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。