|
|
|
|
|
微型真核基因编辑新工具成功研发,基因治疗及育种有新技术了 |
|
|
平均编辑效率较过去提高11倍,将为基因治疗及动植物生物育种提供全新的技术解决方案,这是西北农林科技大学羊遗传改良与生物育种团队联合国内多家单位开发的微型真核基因编辑工具enNlovFz2的亮眼成果。5月20日,关于该新工具的研究论文刊登于国际学术期刊《自然·化学生物学》上。
基因是遗传物质的载体,塑造了生命的多样性和复杂性。基因编辑是理解和改造生命的关键技术,为人类解决多个领域的诸多难题提供了新思路和新方法。基于经典的基因编辑系统CRISPR(成簇规律间隔短回文重复序列)及其衍生技术在功能机制研究、基因治疗及动植物育种等领域应用广泛。然而大部分CRISPR蛋白尺寸较大,难以实现单个腺相关病毒AAV的包装递送,从而限制了其在生物体内编辑的高效应用。
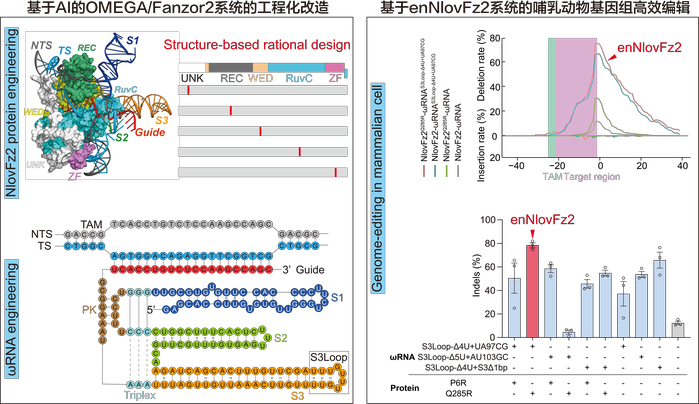 OMEGA/NlovFz2系统的改造与应用。西北农林科技大学供图。
OMEGA/NlovFz2系统的改造与应用。西北农林科技大学供图。
近年来,由RNA(核糖核酸)引导的微型基因编辑工具被陆续发现,推动了基因编辑工具迈入“小型化”时代。基因编辑领域先驱—张锋团队发现了一类新的RNA引导核酸酶,将其命名为“OMEGA系统”,并证实其中源自真核生物的Fanzor蛋白可对人类基因组特定位点进行靶向插入与缺失编辑。与来自原核生物的CRISPR/Cas系统不同,Fanzor源自真核生物,其理论上可以减少动物体内非必要的免疫反应,且保真性强。但是,原始版本的Fanzor系统编辑效率较低(<10%),也限制了其在生物医学和动植物品种改良中的高效应用。
西北农林科技大学羊遗传改良与生物育种团队综合应用基于人工智能的RNA结构优化、蛋白质工程化改造、流式细胞术、全基因组脱靶检测等手段,首次对来源于Fanzor家族的NlovFz2–ωRNA系统进行改造,开发出一种新的微型真核基因编辑工具enNlovFz2,这也是首个基于Fanzor蛋白工具改造的研究报道。
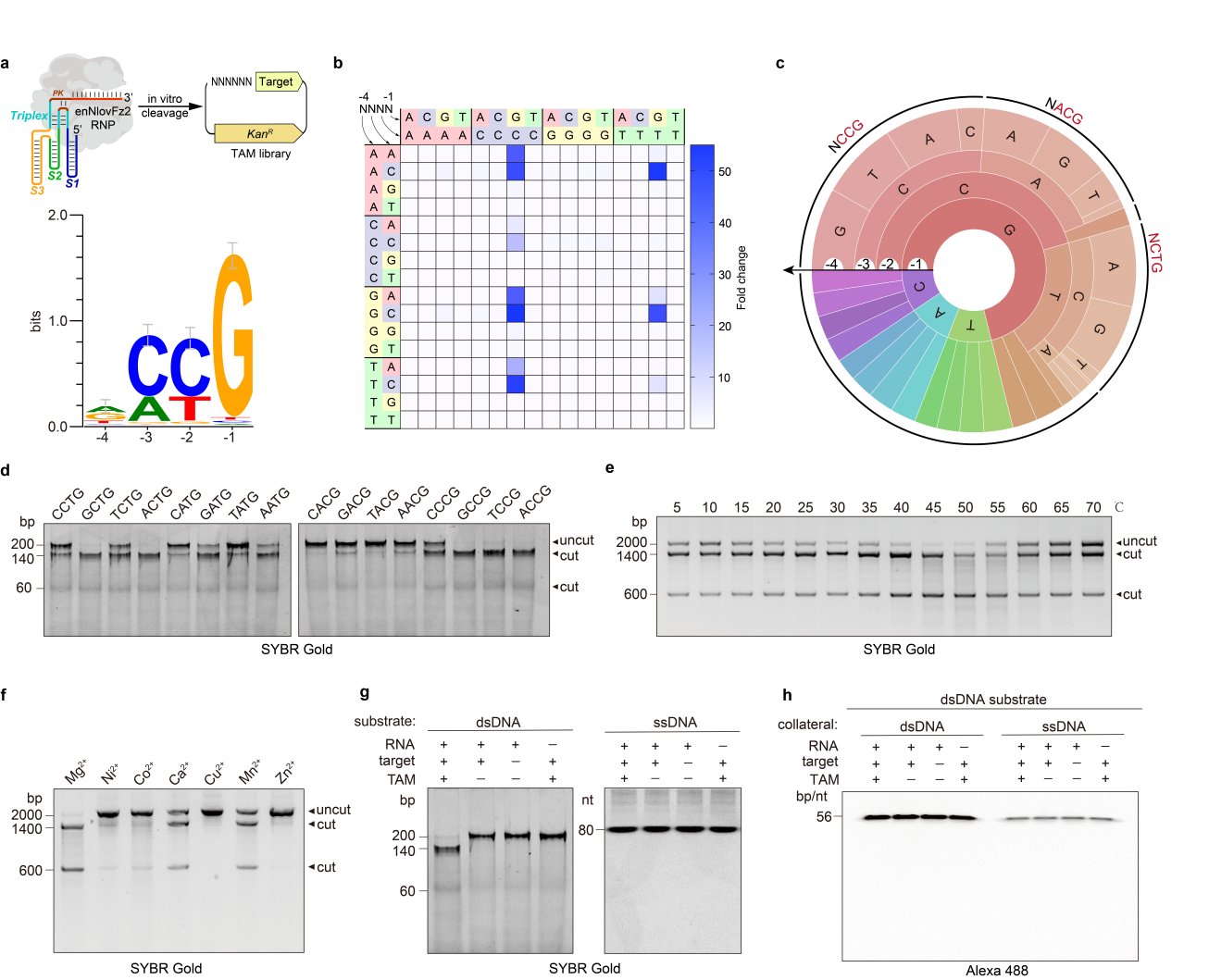 说明:体外生化试验鉴定enNlovFz2的切割特性。西北农林科技大学供图。
说明:体外生化试验鉴定enNlovFz2的切割特性。西北农林科技大学供图。
团队利用该工具对人类基因组的26个靶位点进行了有效编辑,其插入-删除效率高达81.2%,相比原始版本平均编辑效率提高11倍(图1)。相关实验表明,该工具相较于过去,能够识别范围更广的基因序列(图2)。团队利用该工具还成功制备了小鼠白化疾病模型,两个编辑位点体内编辑效率分别达到38.3%和48.7%。同时,在人源化杜氏肌营养不良症(DMD)小鼠疾病模型中,该工具成功并高效将小鼠肌纤维中肌萎缩蛋白水平恢复至野生型小鼠的20%,展现出了广阔的应用前景。
源自真核生物的这一新工具丰富了用于基因组编辑的迷你型核酸酶工具箱,为基因治疗及动植物生物育种提供了高效的候选工具。
西北农林科技大学教授王小龙、副教授徐坤和上海科技大学副研究员吴兆韡为论文的通讯作者,教授魏迎辉、博士研究生高鹏飞、硕士研究生陈宇斐、上海科技大学潘登博士及中国科学院药物研究所李国玲副研究员为论文的共同第一作者,此研究得到农业生物育种重大专项、国家自然科学基金、国家现代农业产业技术体系等资助。
相关论文信息:https://doi.org/10.1038/s41589-025-01902-7
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。