东华大学生物与医学工程学院李静超研究团队,围绕如何通过分子结构调控及多功能化提升抗肿瘤共轭聚合物材料“疗效”和“精度”这一科学问题,提出了一系列创新策略,提升共轭聚合物材料抗肿瘤性能,在癌症精准高效治疗方面取得多项研究进展。相关研究于近日发表在《先进功能材料》和《纳米通讯》。
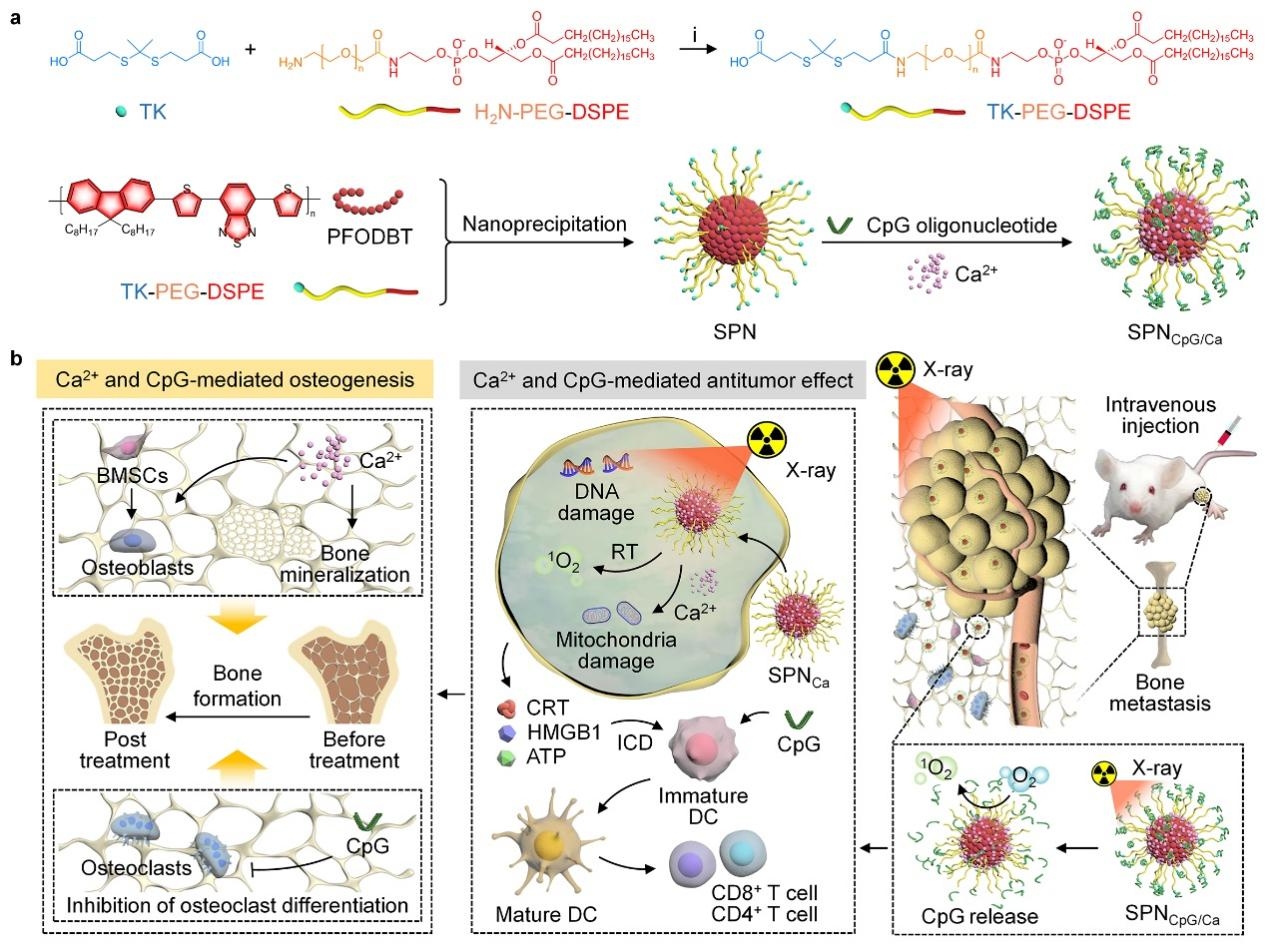
SPNCpG/Ca的合成路线及治疗机制示意图
针对骨转移瘤的治疗难题,李静超研究团队设计了一种多功能半导体纳米整合器(SPNCpG/Ca),通过联合放疗、钙超载以及免疫治疗,实现骨转移瘤的治疗和肿瘤相关骨损伤修复。研究表明,在乳腺癌骨转移小鼠模型中,这种联合治疗策略可有效抑制骨转移瘤的生长和肝肺转移。此外,Ca2+可加速骨髓间充质干细胞成骨分化,而免疫佐剂CpG能够在骨转移微环境中抑制破骨细胞分化来缓解骨溶解,两者协同促进肿瘤相关骨损伤的修复。这种多功能的治疗性纳米系统,具有治疗骨转移和修复肿瘤相关骨损伤的能力,为骨转移的治疗提供了新策略。
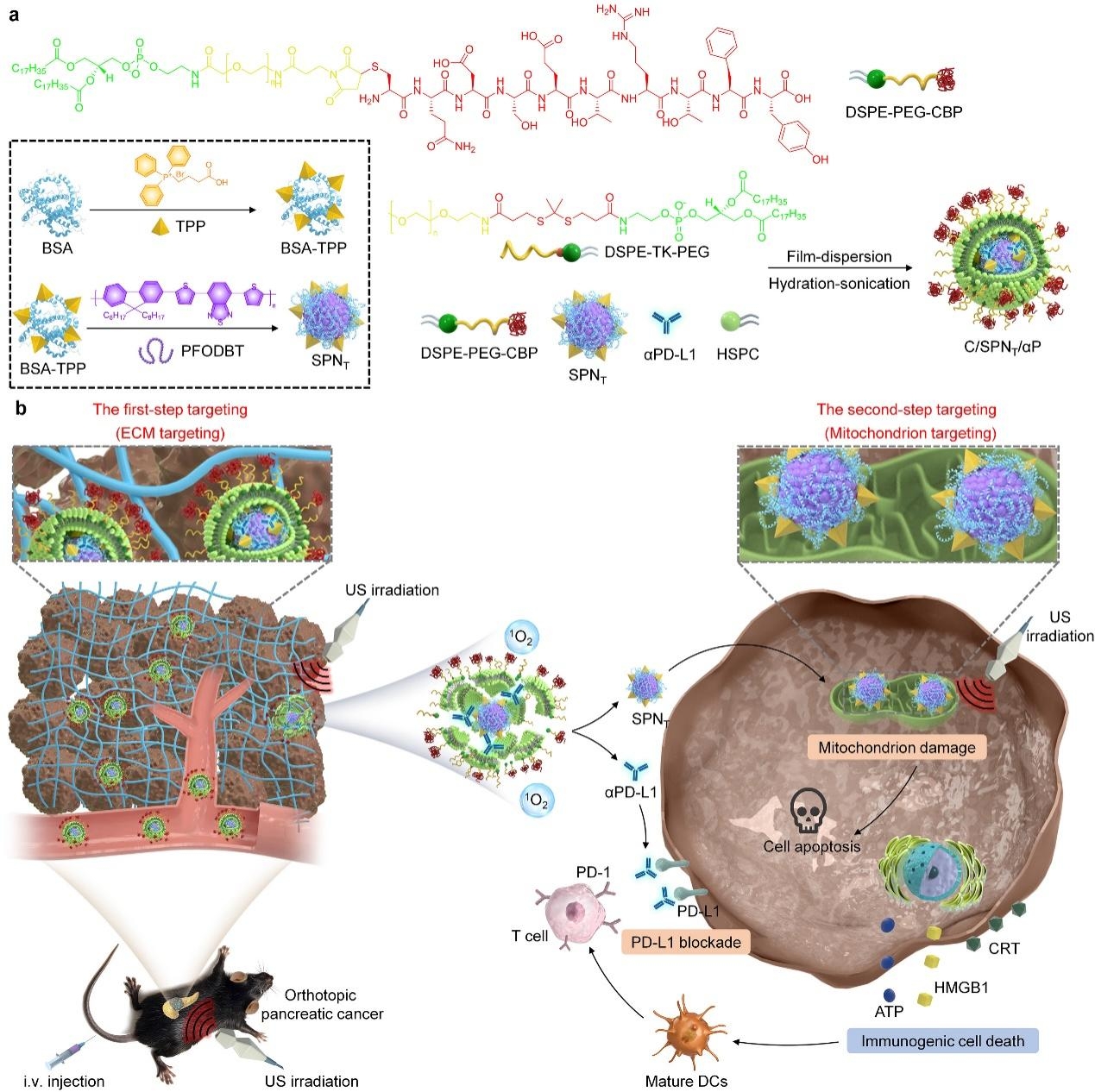
两步靶向可调型C/SPNT/αP的合成路线及治疗原位胰腺癌示意图
针对胰腺癌临床治疗困境,李静超研究团队设计了一种半导体纳米转换器(C/SPNT/αP),通过放大线粒体损伤和程序性死亡配体1(PD-L1)阻断,实现原位胰腺癌治疗。新型的治疗策略可以有效治疗小鼠原位胰腺Panc02和KPC模型肿瘤。
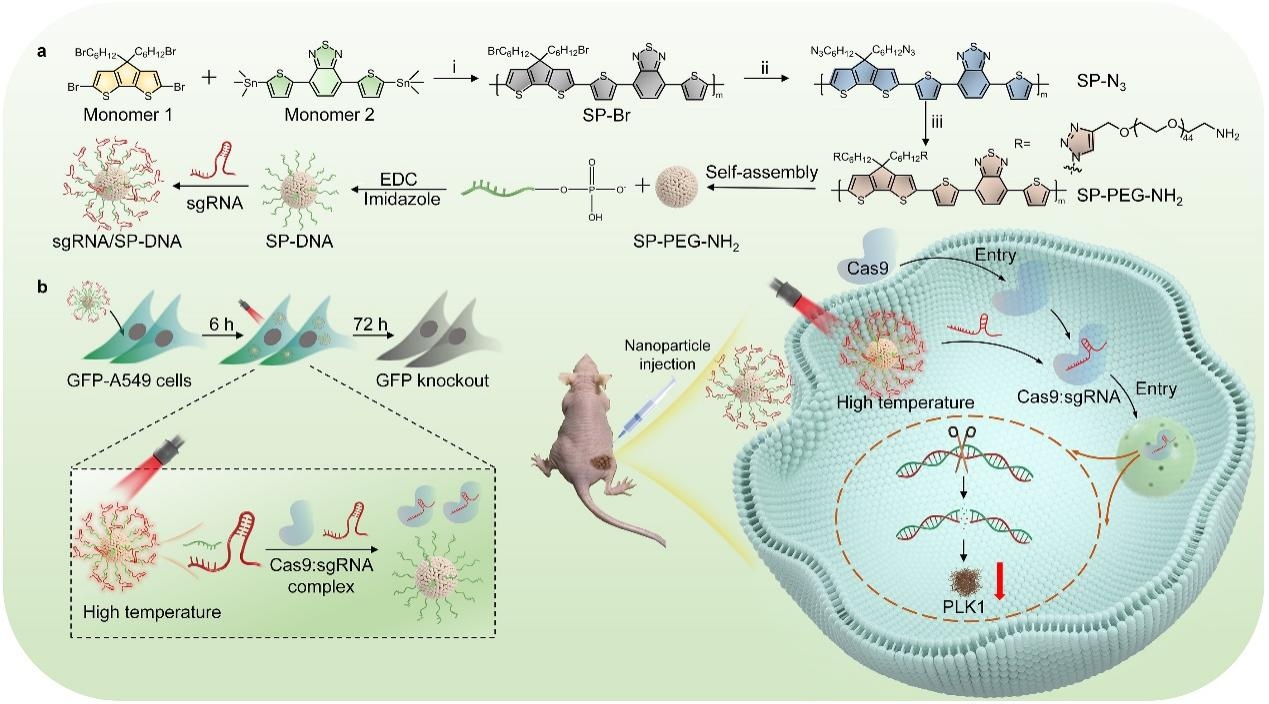
NIR光响应型有机高分子纳米载体用于CRISPR活性调控和肿瘤基因治疗示意图。图片均由研究团队提供
针对“如何实现CRISPR在病灶部位的特异性富集且避免脱靶效应”这一临床转化关键问题,李静超研究团队构建了基于半导体聚合物构建NIR光响应型有机高分子纳米载体用于CRISPR活性调控和肿瘤基因治疗。研究团队发现,该纳米载体在履行递送职责的同时,可作为NIR光热转换媒介将光能转换为热能,导致sgRNA/SP-DNA纳米体系附近局部温度升高,sgRNA与单链DNA解链,释放出自由的sgRNA,从而实现对CRISPR/Cas9活性的精准调控。
相关论文链接:https://doi.org/10.1002/adfm.202412165
https://doi.org/10.1002/adfm.202413233
https://doi.org/10.1021/acs.nanolett.5c00285
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。