近日,南方医科大学南方医院教授潘速跃/黄凯滨团队研究揭示了心脏骤停幸存者脑损伤的关键机制,肠道来源巨噬细胞向脑内浸润通过引发神经炎症在其中起着关键作用。相关成果发表于《细胞与分子免疫学杂志》(Cellular & Molecular Immunology)。
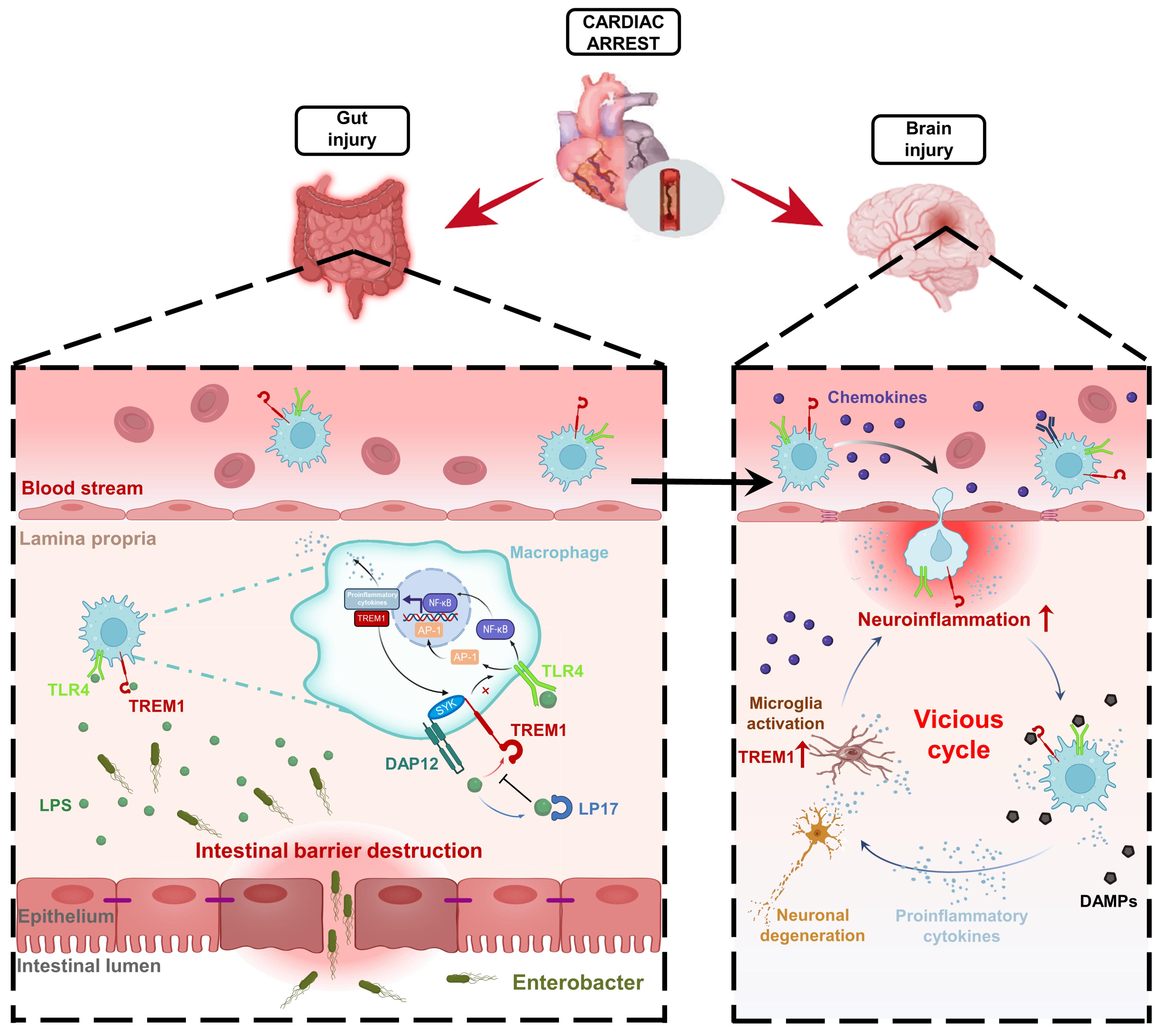 心肺复苏后肠道巨噬细胞装载TREM1信号,迁移入脑后放大神经炎症反应示意图。研究团队 供图
心肺复苏后肠道巨噬细胞装载TREM1信号,迁移入脑后放大神经炎症反应示意图。研究团队 供图
?
脑损伤是心脏骤停幸存者的主要致死和致残原因,但其具体病理机制尚未明确。该研究团队构建小鼠心脏骤停/心肺复苏模型,创新性采用活体光转化示踪技术,首次证实小肠巨噬细胞在心脏骤停后向脑实质的大规模迁移现象。多组学分析发现:浸润脑组织的肠源性巨噬细胞特异性高表达髓细胞触发受体1(TREM1);心脏骤停后肠道菌群显著失衡,肠杆菌科异常增殖导致脂多糖释放,通过激活TLR4-TREM1信号轴驱动神经炎症。关键机制验证显示,靶向阻断TREM1可显著改善脑损伤,且临床队列证实TREM1表达水平与患者不良神经预后呈显著正相关。
该研究首次确立肠源性巨噬细胞作为心脏骤停后神经炎症的关键效应细胞,并揭示了“肠道菌群紊乱-多糖释放-TREM1激活”的跨器官级联反应机制。同时确立TREM1作为连接肠脑轴的核心分子靶点。
论文共同通讯作者潘速跃表示,该研究突破传统中枢神经炎症研究范式,从肠脑互作角度提出心脏骤停后脑损伤的“二次打击”理论:原发缺血损伤后,肠道菌群失调引发的外周TREM1+巨噬细胞脑浸润构成神经炎症持续恶化的关键环节。
该发现具有重要转化价值:TREM1信号靶点的确定,为开发LP17等选择性抑制剂提供理论依据。研究策略可拓展至卒中、创伤性脑损伤等涉及肠脑轴紊乱的神经系统疾病,为精准干预开辟新方向。
相关论文信息:https://doi.org/10.1038/s41423-025-01263-0
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。