|
|
|
|
|
科学家“看到”调控学习和记忆“分子开关”的精细结构 |
|
|
中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)研究员竺淑佳课题组与中国科学院上海药物研究所研究员李扬课题组合作,首次在原子分辨率上“看到”调控哺乳动物学习和记忆的“分子开关”的精细结构,揭示了内源N-甲基-?-天冬氨酸(NDMA)受体的原子分辨率三维结构,突破了NMDA受体的分子结构与功能研究局限于异源重组表达系统的瓶颈,为开发靶向NMDA受体治疗神经或精神类疾病的新型药物提供了重要的理论基础。1月23日,相关研究发表于《细胞》。
NMDA受体是一类存在于突触上的离子型谷氨酸门控通道家族,广泛参与神经发育、突触可塑性、学习记忆、认知及情绪等高级脑功能调控,被视为学习和记忆的关键“分子开关”。近年来的临床医学研究揭示,NMDA受体功能障碍与一系列神经精神疾病密切相关。因此,NMDA受体一直是神经科学领域药物设计的热门靶点,已有靶向NMDA受体的分子用于临床抑郁症和阿尔茨海默症的治疗。
在哺乳动物中,NMDA受体由7个基因编码的7个不同亚基组成,功能性NMDA受体通常由两个必需的GluN1亚基和两个可变的GluN2/3(N2A-N2D,N3A-N3B)亚基组装形成二异或三异四聚体。然而,大脑内源NMDA受体的亚基表达和受体组装受到严格的时空调控,许多问题都尚未解答,极大限制了对突触功能的理解。
基于自主开发的靶向各个NMDA受体亚基的构象特异性单克隆抗体,研究团队成功从成年大鼠的大脑皮层和海马中富集和分离出了丰度极低的内源NMDA受体。
通过冷冻电镜(cryo-EM)技术,团队解析出了3种主要的受体亚型,它们分别以45%,35%和20%的比例构成了皮层和海马中的内源NMDA受体。其中,GluN1-N2A-N2B三异四聚体作为内源丰度最高亚型的发现,更新了领域内三十年来以GluN1-N2A和GluN1-N2B二异四聚体为主要亚型的观念,强调了GluN2A和GluN2B亚基在生理状态同一受体中的功能整合。
研究团队进一步通过结构对比发现了GluN2B亚基在GluN1-N2A-N2B三异四聚体和GluN1-N2B二异四聚体中的构象区别,揭示了同一亚基在不同受体中存在构象差异,进而决定了不同亚型的生物物理学、药理学和通道开放属性。
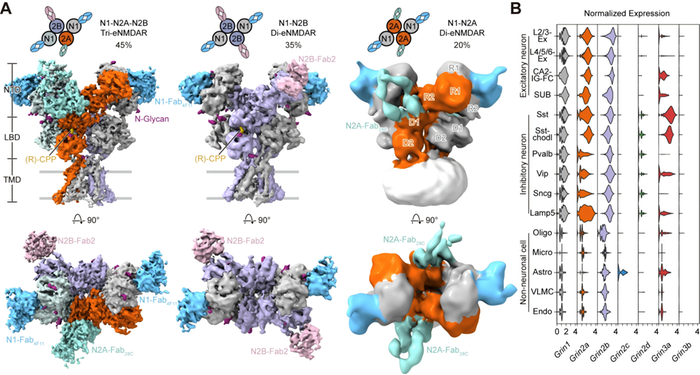 皮层和海马内源NMDA受体的主要亚型和不同亚基在单细胞转录组水平上的分布。图片来源于《细胞》
皮层和海马内源NMDA受体的主要亚型和不同亚基在单细胞转录组水平上的分布。图片来源于《细胞》
?
研究团队表示,不同内源NMDA受体间的构象差异,为理解内源NMDA受体的功能多样性,以及不同受体的药理差异提供了分子基础。这一发现为设计具有亚基特异性且具有亚型偏好性的化合物提供了可能,有助于提高NMDA受体药物的靶向性。
相关论文信息:https://doi.org/10.1016/j.cell.2025.01.004
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。