11月25日,西湖大学多维动态代谢组学核心实验室主任邹贻龙课题组、西湖大学基因组学与生物信息学核心实验室主任王曦课题组在《细胞》上发表文章,系统性地解析了支撑卵巢癌远端转移的代谢基础,并深入揭示不饱和脂质在肿瘤转移的各个阶段起到的多重作用。
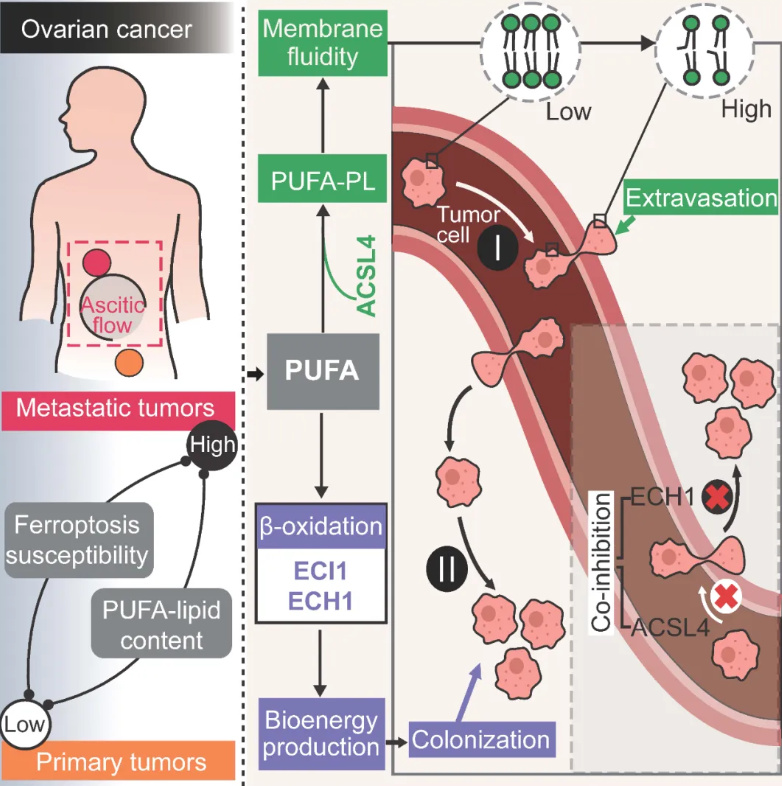 研究揭示不饱和脂质代谢网络在肿瘤转移的血运扩散和远端器官定植生长等环节中发挥的双重作用。课题组供图
研究揭示不饱和脂质代谢网络在肿瘤转移的血运扩散和远端器官定植生长等环节中发挥的双重作用。课题组供图
?
他们证实了ACSL4与和ECH1是影响卵巢癌转移中的关键因子。鉴于不饱和脂肪酸代谢在肿瘤细胞血管外渗和体内生长过程中的双重作用,研究人员在多种肿瘤转移模型中联合敲除了ACSL4和ECH1的表达,同时抑制住了肿瘤细胞在远端器官的定植和生长,成功控制了肿瘤细胞整体的血运转移负担。
这项研究成果系统性地挖掘了肿瘤转移相关的化合物敏感性,构建了转移瘤相关原代细胞培养体系和动物模型,为肿瘤转移的机制研究提供了资源和模型。同时,它通过体内CRISPR功能基因组学筛选,揭示了多条在肿瘤多路径转移过程中发挥作用的代谢通路,提供了潜在的抗肿瘤转移靶点。
它还深入揭示了不饱和脂质代谢通路在肿瘤血运转移中的突出贡献,发现这一作用在多个癌种中的可推广性,为透彻理解肿瘤转移的代谢调控机制提供了新的视角。
研究为抗肿瘤转移的治疗提供了潜在的药物靶点。“更重要的是,由于该机理适用于多种癌症,这些发现将能帮助人们更透彻理解肿瘤转移的代谢调控机制,开发针对包括卵巢癌在内的多种癌症的转移药物。”邹贻龙说。
相关论文信息:https://doi.org/10.1016/j.cell.2024.10.047
版权声明:凡本网注明“来源:中国科学报、科学网、科学新闻杂志”的所有作品,网站转载,请在正文上方注明来源和作者,且不得对内容作实质性改动;微信公众号、头条号等新媒体平台,转载请联系授权。邮箱:shouquan@stimes.cn。